Questões de Química - Equilíbrio Químico para Concurso
Foram encontradas 267 questões
Observe a figura abaixo e considere a seguinte reação de eletrólise de NaCI aquoso 1 mol L-1:
Semicélula: 2Cl-(aq) → Cl2(g) + 2e-
Semicélula: 2e- + 2H2O → H2(g) + 2OH-(aq)
Célula: 2H2O(aq) + 2Cl-(aq) → H2(g) + Cl2(g) + 2OH-(aq)
Com base nas informações pode-se afirmar que:
O pH dessa solução é
Dado log 3 = 0,5
PbSO4 (s) ⇌ Pb2+(aq) + SO2–4 (aq)
A constante de equilíbrio (Kps) para essa reação é conhecida e equivale a 1,0 × 10−8 . Com base no equilíbrio iônico de solubilidade, a concentração máxima de íons de chumbo (Pb²⁺) na água tratada antes que o PbSO₄ comece a precipitar será de:
As antocianinas e seus derivados são pigmentos naturais polares da classe de compostos orgânicos chamados flavonoides e estão presentes nas uvas, sendo responsáveis pela cor do vinho tinto. Tais pigmentos são substâncias fenólicas que podem ter diversas cores, como vermelha, roxa, azul, e podem ser encontrados também em pétalas de flores, framboesa, figo, cereja, amora, beterraba, romã, maçã, cebola roxa, repolho roxo entre outros. O extrato aquoso obtido a partir do repolho roxo tem cor roxa e pH 7, a
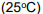 , contém antocianinas e pode apresentar o
seguinte comportamento a partir da adição de gotas de
soluções aquosas de substâncias com os seguintes valores
de pH:
, contém antocianinas e pode apresentar o
seguinte comportamento a partir da adição de gotas de
soluções aquosas de substâncias com os seguintes valores
de pH: 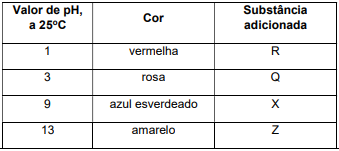
Pode-se verificar então que o extrato aquoso de repolho roxo funciona como um indicador de pH. A solução aquosa da substância R, adicionada a este extrato, pode ser de