Questões de Concurso Público MPU 2015 para Analista do MPU - Engenharia Química
Foram encontradas 6 questões
Ano: 2015
Banca:
CESPE / CEBRASPE
Órgão:
MPU
Prova:
CESPE - 2015 - MPU - Analista do MPU - Engenharia Química |
Q489950
Engenharia Química e Química Industrial
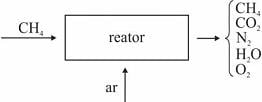
Em um reator ideal, de processo contínuo, que opera em estado estacionário, a combustão de
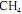 ocorre com uma conversão de 90% do reagente limitante. Esse reator é alimentado com
ocorre com uma conversão de 90% do reagente limitante. Esse reator é alimentado com 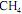 e ar a taxas de 16 kg/h e 300 kg/h, respectivamente, conforme ilustrado no esquema apresentado.
e ar a taxas de 16 kg/h e 300 kg/h, respectivamente, conforme ilustrado no esquema apresentado. Considerando que, nessa situação, a combustão do
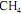 seja completa e que a composição do ar que alimenta o reator seja de 24%, em massa, de
seja completa e que a composição do ar que alimenta o reator seja de 24%, em massa, de 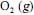 e, o restante, de
e, o restante, de 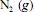 , julgue o item subsequente.
, julgue o item subsequente.A porcentagem, em massa, de
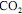 na corrente de saída do reator é superior a 10%.
na corrente de saída do reator é superior a 10%.
Ano: 2015
Banca:
CESPE / CEBRASPE
Órgão:
MPU
Prova:
CESPE - 2015 - MPU - Analista do MPU - Engenharia Química |
Q489957
Engenharia Química e Química Industrial
Texto associado
O  , obtido como subproduto da eletrólise do
, obtido como subproduto da eletrólise do  , é largamente empregado na indústria em reações de hidrogenação, como a que ocorre com o eteno
, é largamente empregado na indústria em reações de hidrogenação, como a que ocorre com o eteno  , representada pela seguinte
, representada pela seguinte
equação:

A tabela seguinte contém as energias livres de Gibbs padrão de formação a 25 ºC de cada composto envolvido.
a 25 ºC de cada composto envolvido.

O gráfico a seguir mostra o ln da constante de velocidade da referida reação (k) em função do inverso da temperatura (1/T) para a reação catalisada por dois diferentes metais.

 , obtido como subproduto da eletrólise do
, obtido como subproduto da eletrólise do  , é largamente empregado na indústria em reações de hidrogenação, como a que ocorre com o eteno
, é largamente empregado na indústria em reações de hidrogenação, como a que ocorre com o eteno  , representada pela seguinte
, representada pela seguinteequação:

A tabela seguinte contém as energias livres de Gibbs padrão de formação
 a 25 ºC de cada composto envolvido.
a 25 ºC de cada composto envolvido.
O gráfico a seguir mostra o ln da constante de velocidade da referida reação (k) em função do inverso da temperatura (1/T) para a reação catalisada por dois diferentes metais.

Considerando que as reações de hidrogenação sejam exotérmicas, que todos os gases envolvidos apresentem comportamento ideal e que o produto da constante universal dos gases pela temperatura absoluta (R×T) seja igual a 2.500 J/mol, julgue o item que se segue.
A constante de equilíbrio para a reação de hidrogenação do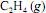 a 100 ºC é maior que a 25 ºC.
a 100 ºC é maior que a 25 ºC.
A constante de equilíbrio para a reação de hidrogenação do
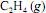 a 100 ºC é maior que a 25 ºC.
a 100 ºC é maior que a 25 ºC.
Ano: 2015
Banca:
CESPE / CEBRASPE
Órgão:
MPU
Prova:
CESPE - 2015 - MPU - Analista do MPU - Engenharia Química |
Q489958
Engenharia Química e Química Industrial
Texto associado
O  , obtido como subproduto da eletrólise do
, obtido como subproduto da eletrólise do  , é largamente empregado na indústria em reações de hidrogenação, como a que ocorre com o eteno
, é largamente empregado na indústria em reações de hidrogenação, como a que ocorre com o eteno  , representada pela seguinte
, representada pela seguinte
equação:

A tabela seguinte contém as energias livres de Gibbs padrão de formação a 25 ºC de cada composto envolvido.
a 25 ºC de cada composto envolvido.

O gráfico a seguir mostra o ln da constante de velocidade da referida reação (k) em função do inverso da temperatura (1/T) para a reação catalisada por dois diferentes metais.

 , obtido como subproduto da eletrólise do
, obtido como subproduto da eletrólise do  , é largamente empregado na indústria em reações de hidrogenação, como a que ocorre com o eteno
, é largamente empregado na indústria em reações de hidrogenação, como a que ocorre com o eteno  , representada pela seguinte
, representada pela seguinteequação:

A tabela seguinte contém as energias livres de Gibbs padrão de formação
 a 25 ºC de cada composto envolvido.
a 25 ºC de cada composto envolvido.
O gráfico a seguir mostra o ln da constante de velocidade da referida reação (k) em função do inverso da temperatura (1/T) para a reação catalisada por dois diferentes metais.

Considerando que as reações de hidrogenação sejam exotérmicas, que todos os gases envolvidos apresentem comportamento ideal e que o produto da constante universal dos gases pela temperatura absoluta (R×T) seja igual a 2.500 J/mol, julgue o item que se segue.
Sob determinada temperatura, a reação de hidrogenação do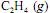 liberará maior quantidade de calor se realizada a volume constante, e não a pressão constante.
liberará maior quantidade de calor se realizada a volume constante, e não a pressão constante.
Sob determinada temperatura, a reação de hidrogenação do
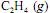 liberará maior quantidade de calor se realizada a volume constante, e não a pressão constante.
liberará maior quantidade de calor se realizada a volume constante, e não a pressão constante.
Ano: 2015
Banca:
CESPE / CEBRASPE
Órgão:
MPU
Prova:
CESPE - 2015 - MPU - Analista do MPU - Engenharia Química |
Q489959
Engenharia Química e Química Industrial
Texto associado
O  , obtido como subproduto da eletrólise do
, obtido como subproduto da eletrólise do  , é largamente empregado na indústria em reações de hidrogenação, como a que ocorre com o eteno
, é largamente empregado na indústria em reações de hidrogenação, como a que ocorre com o eteno  , representada pela seguinte
, representada pela seguinte
equação:

A tabela seguinte contém as energias livres de Gibbs padrão de formação a 25 ºC de cada composto envolvido.
a 25 ºC de cada composto envolvido.

O gráfico a seguir mostra o ln da constante de velocidade da referida reação (k) em função do inverso da temperatura (1/T) para a reação catalisada por dois diferentes metais.

 , obtido como subproduto da eletrólise do
, obtido como subproduto da eletrólise do  , é largamente empregado na indústria em reações de hidrogenação, como a que ocorre com o eteno
, é largamente empregado na indústria em reações de hidrogenação, como a que ocorre com o eteno  , representada pela seguinte
, representada pela seguinteequação:

A tabela seguinte contém as energias livres de Gibbs padrão de formação
 a 25 ºC de cada composto envolvido.
a 25 ºC de cada composto envolvido.
O gráfico a seguir mostra o ln da constante de velocidade da referida reação (k) em função do inverso da temperatura (1/T) para a reação catalisada por dois diferentes metais.

Considerando que as reações de hidrogenação sejam exotérmicas, que todos os gases envolvidos apresentem comportamento ideal e que o produto da constante universal dos gases pela temperatura absoluta (R×T) seja igual a 2.500 J/mol, julgue o item que se segue.
A energia de ativação da reação de hidrogenação catalisada pelo metal B é superior à da reação catalisada pelo metal A.
A energia de ativação da reação de hidrogenação catalisada pelo metal B é superior à da reação catalisada pelo metal A.
Ano: 2015
Banca:
CESPE / CEBRASPE
Órgão:
MPU
Prova:
CESPE - 2015 - MPU - Analista do MPU - Engenharia Química |
Q489960
Engenharia Química e Química Industrial
Texto associado
O  , obtido como subproduto da eletrólise do
, obtido como subproduto da eletrólise do  , é largamente empregado na indústria em reações de hidrogenação, como a que ocorre com o eteno
, é largamente empregado na indústria em reações de hidrogenação, como a que ocorre com o eteno  , representada pela seguinte
, representada pela seguinte
equação:

A tabela seguinte contém as energias livres de Gibbs padrão de formação a 25 ºC de cada composto envolvido.
a 25 ºC de cada composto envolvido.

O gráfico a seguir mostra o ln da constante de velocidade da referida reação (k) em função do inverso da temperatura (1/T) para a reação catalisada por dois diferentes metais.

 , obtido como subproduto da eletrólise do
, obtido como subproduto da eletrólise do  , é largamente empregado na indústria em reações de hidrogenação, como a que ocorre com o eteno
, é largamente empregado na indústria em reações de hidrogenação, como a que ocorre com o eteno  , representada pela seguinte
, representada pela seguinteequação:

A tabela seguinte contém as energias livres de Gibbs padrão de formação
 a 25 ºC de cada composto envolvido.
a 25 ºC de cada composto envolvido.
O gráfico a seguir mostra o ln da constante de velocidade da referida reação (k) em função do inverso da temperatura (1/T) para a reação catalisada por dois diferentes metais.

Considerando que as reações de hidrogenação sejam exotérmicas, que todos os gases envolvidos apresentem comportamento ideal e que o produto da constante universal dos gases pela temperatura absoluta (R×T) seja igual a 2.500 J/mol, julgue o item que se segue.
Considere que a reação de hidrogenação em apreço seja de ordem um com relação ao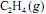 e de ordem um com relação ao
e de ordem um com relação ao 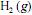 , e que as concentrações iniciais de cada um dos dois reagentes sejam iguais a
, e que as concentrações iniciais de cada um dos dois reagentes sejam iguais a  . Nessas condições, a concentração de
. Nessas condições, a concentração de 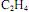 em um instante t da reação é dada por
em um instante t da reação é dada por 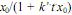 , em que k' é a constante de velocidade na temperatura da reação.
, em que k' é a constante de velocidade na temperatura da reação.
Considere que a reação de hidrogenação em apreço seja de ordem um com relação ao
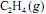 e de ordem um com relação ao
e de ordem um com relação ao 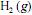 , e que as concentrações iniciais de cada um dos dois reagentes sejam iguais a
, e que as concentrações iniciais de cada um dos dois reagentes sejam iguais a  . Nessas condições, a concentração de
. Nessas condições, a concentração de 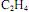 em um instante t da reação é dada por
em um instante t da reação é dada por 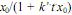 , em que k' é a constante de velocidade na temperatura da reação.
, em que k' é a constante de velocidade na temperatura da reação.