Questões de Concurso Público IF-PR 2014 para Técnico em Laboratório - Química
Foram encontradas 2 questões
Ano: 2014
Banca:
CETRO
Órgão:
IF-PR
Prova:
CETRO - 2014 - IF-PR - Técnico em Laboratório - Química |
Q454950
Química
Observe os efeitos do deslocamento do equilíbrio químico que ocorre em duas soluções, cujos sistemas apresentam as respectivas equações de equilíbrio:
Equação de Equilíbrio da Solução 1:
2 CrO4-2 (aq) + 4 H+ (aq) Cr2O7 -2(aq) + 2 H2O (l)
Cr2O7 -2(aq) + 2 H2O (l)
Equação de Equilíbrio da Solução 2:
[CoCl 4] -2 (aq) + 4H2O(l) [Co(H2O)4Cl 2](aq) + 2 Cl-(l) ΔH<0
[Co(H2O)4Cl 2](aq) + 2 Cl-(l) ΔH<0
Com base nas informações acima, foram feitos quatro experimentos, com as duas soluções, levando-se em conta as condições para observação do deslocamento do equilíbrio químico. Os resultados foram tabelados abaixo.
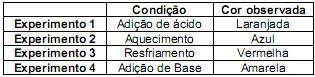
São informações corretas a respeito do estudo efetuado acima, exceto uma. Assinale a alternativa que a apresenta.
Equação de Equilíbrio da Solução 1:
2 CrO4-2 (aq) + 4 H+ (aq)
 Cr2O7 -2(aq) + 2 H2O (l)
Cr2O7 -2(aq) + 2 H2O (l) Equação de Equilíbrio da Solução 2:
[CoCl 4] -2 (aq) + 4H2O(l)
 [Co(H2O)4Cl 2](aq) + 2 Cl-(l) ΔH<0
[Co(H2O)4Cl 2](aq) + 2 Cl-(l) ΔH<0 Com base nas informações acima, foram feitos quatro experimentos, com as duas soluções, levando-se em conta as condições para observação do deslocamento do equilíbrio químico. Os resultados foram tabelados abaixo.

São informações corretas a respeito do estudo efetuado acima, exceto uma. Assinale a alternativa que a apresenta.
Ano: 2014
Banca:
CETRO
Órgão:
IF-PR
Prova:
CETRO - 2014 - IF-PR - Técnico em Laboratório - Química |
Q454964
Química
Experimentos revelam que nem todas as reações químicas são irreversíveis. Por exemplo, o tetróxido de nitrogênio (N2O4), que é uma substância incolor, decompõe-se facilmente e de forma reversível, formando dióxido de nitrogênio (NO2), que, por sua vez, é uma substância de cor avermelhada. A equação não balanceada abaixo representa a decomposição descrita.
N2O4(g)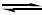 NO2(g)
NO2(g)
Utilizando uma seringa com a ponta fechada, na qual continha uma mistura destas substâncias em estados de equilíbrio químico, no estado físico gasoso, um estudante fez o experimento observando diferenças significativas de coloração. O experimento encontra-se esquematizado abaixo, sendo que (1) representa o estado de equilíbrio químico inicial e (2), o estado de equilíbrio químico final.
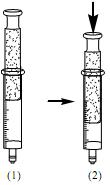
Tendo em vista o estado inicial (1) e o final (2), e que cada um destes estados apresenta uma coloração diferente em estado de equilíbrio, é correto afirmar que o estudante, ao pressionar o pistão da seringa, concluiu que
N2O4(g)
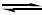 NO2(g)
NO2(g) Utilizando uma seringa com a ponta fechada, na qual continha uma mistura destas substâncias em estados de equilíbrio químico, no estado físico gasoso, um estudante fez o experimento observando diferenças significativas de coloração. O experimento encontra-se esquematizado abaixo, sendo que (1) representa o estado de equilíbrio químico inicial e (2), o estado de equilíbrio químico final.

Tendo em vista o estado inicial (1) e o final (2), e que cada um destes estados apresenta uma coloração diferente em estado de equilíbrio, é correto afirmar que o estudante, ao pressionar o pistão da seringa, concluiu que