Questões de Concurso Público UFPI 2023 para Técnico de Laboratório - Química
Foram encontradas 4 questões
Ano: 2023
Banca:
COPESE - UFPI
Órgão:
UFPI
Prova:
COPESE - UFPI - 2023 - UFPI - Técnico de Laboratório - Química |
Q2210808
Química
As estruturas de cristais de sólidos iônicos binários podem ser racionalizadas como um empacotamento de
átomos de um dos elementos, estando os átomos do segundo elemento preenchendo os buracos (interstícios)
formados pelo primeiro. Considere uma célula unitária cúbica de face centrada de um composto iônico com
fórmula XY (Figura abaixo). Na estrutura mostrada, as esferas mais claras representam o elemento Y e os sítios
marcados com esferas pretas representam os interstícios tetraédricos (como pode ser visto pelo tetraedro
desenhado dentro da célula unitária).
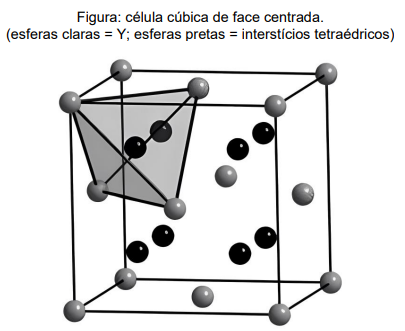
Sabe-se que, na célula apresentada, 1/8 (um oitavo) dos elementos nos vértices contribuem efetivamente para o retículo, enquanto os elementos nas faces contribuem com 1/2 (um meio). Diante das informações citadas, assinale a opção que mostra o número de INTERSTÍCIOS TETRAÉDRICOS, na célula cúbica mostrada, OCUPADOS PELO ELEMENTO X:

Sabe-se que, na célula apresentada, 1/8 (um oitavo) dos elementos nos vértices contribuem efetivamente para o retículo, enquanto os elementos nas faces contribuem com 1/2 (um meio). Diante das informações citadas, assinale a opção que mostra o número de INTERSTÍCIOS TETRAÉDRICOS, na célula cúbica mostrada, OCUPADOS PELO ELEMENTO X:
Ano: 2023
Banca:
COPESE - UFPI
Órgão:
UFPI
Prova:
COPESE - UFPI - 2023 - UFPI - Técnico de Laboratório - Química |
Q2210812
Química
Dadas as afirmações abaixo, julgue-as como Verdadeira (V) ou Falsa (F).
I. A uma temperatura fixa, uma solução aquosa saturada de um determinado soluto sempre contém uma quantidade fixa desse soluto;
II. Todos os líquidos fervem a uma temperatura superior ao seu ponto de ebulição normal quando contêm impurezas não voláteis;
III. Toda solução comporta-se como uma solução ideal.
Com base na análise dos itens I, II e III, assinale a opção CORRETA:
I. A uma temperatura fixa, uma solução aquosa saturada de um determinado soluto sempre contém uma quantidade fixa desse soluto;
II. Todos os líquidos fervem a uma temperatura superior ao seu ponto de ebulição normal quando contêm impurezas não voláteis;
III. Toda solução comporta-se como uma solução ideal.
Com base na análise dos itens I, II e III, assinale a opção CORRETA:
Ano: 2023
Banca:
COPESE - UFPI
Órgão:
UFPI
Prova:
COPESE - UFPI - 2023 - UFPI - Técnico de Laboratório - Química |
Q2210822
Química
Uma mistura salina de 1,2 g, contendo os sais A2CO3, AHCO3 e ACl foi dissolvida em 100 mL de água. Uma
alíquota de 10 mL dessa solução precisou de 7,00 mL de uma solução de HCl 0,167 mol/L para alcançar o ponto
final numa titulação, utilizando o alaranjado de metila como indicador. Em uma análise separada, uma alíquota
de 25 mL da mesma solução foi adicionada a 20 mL de NaOH 0,1 mol/L e, em seguida, foi adicionado um
excesso de solução de BaCl2. A solução resultante foi filtrada e foram necessários 15 mL de H2SO4 0,025 mol/L
para a completa neutralização. Diante das informações, assinale a opção que mostra as porcentagens em
massa de cada sal na mistura original:
Dados eventualmente necessários: massas molares (g/mol): A = 23; C = 12; O = 16; Cl = 35,5; H = 1.
Dados eventualmente necessários: massas molares (g/mol): A = 23; C = 12; O = 16; Cl = 35,5; H = 1.
Ano: 2023
Banca:
COPESE - UFPI
Órgão:
UFPI
Prova:
COPESE - UFPI - 2023 - UFPI - Técnico de Laboratório - Química |
Q2210824
Química
Madame Bovary ou Emma Bovary é a personagem principal do romance francês escrito por Gustave Flaubert
(1821-1880), publicado em 1856. No livro, ela morre por envenenamento com arsênio (elemento da coluna 15 da
Tabela Periódica), após ter um caso amoroso e se endividar. De fato, o “envenenamento por arsênio” ocupa
lugar importante tanto no imaginário literário quanto na própria história humana, haja vista as especulações
relacionadas às mortes de Napoleão Bonaparte (1769-1821), da rainha Caroline Matilda da Dinamarca (1751-
1775) e do rei George III do Reino Unido (1738-1820). Um dos teste de detecção de arsênio pode ser aplicado a
um dos seus minérios, a arsenolita, As2O3. Neste teste, há três etapas: 1) o óxido é misturado com ácido
clorídrico e zinco sólido. Ocorre a formação de cloreto de zinco, água e arsina (AsH3), um gás tóxico; 2) o gás é
aquecido formando hidrogênio e um material escuro brilhante, que é arsênio elementar; e 3) este último é
dissolvido com solução de hipoclorito de sódio, gerando ácido arsênico.
Após a leitura, assinale a opção que mostra O SOMATÓRIO DOS COEFICIENTES ESTEQUIOMÉTRICOS, expressos com os menores inteiros, da reação citada na etapa 1 acima, A GEOMETRIA MOLECULAR da arsina e o ESTADO DE OXIDAÇÃO (Nox) do arsênio no ácido arsênico, respectivamente:
Após a leitura, assinale a opção que mostra O SOMATÓRIO DOS COEFICIENTES ESTEQUIOMÉTRICOS, expressos com os menores inteiros, da reação citada na etapa 1 acima, A GEOMETRIA MOLECULAR da arsina e o ESTADO DE OXIDAÇÃO (Nox) do arsênio no ácido arsênico, respectivamente: