Questões de Concurso Público IF-RS 2023 para Professor - Química
Foram encontradas 17 questões
Q2358164
Química
Sobre ligações químicas, analise as assertivas a seguir assinale V, se verdadeiras, ou
F, se falsas.
( ) A teoria dos orbitais moleculares é a que melhor descreve a ligação química, pois resolve as deficiências da Teoria de Lewis e é mais simples na utilização dos cálculos quando comparada à Teoria de Valência.
( ) Nas ligações múltiplas, um átomo forma uma ligação “sigma” usando um orbital híbrido (sp ou sp2 ) e uma ou mais ligações “pi” usando orbitais não hibridados. A superposição lateral que produz uma ligação “pi” não restringe a rotação das moléculas, resultando em ligações mais fracas do que as ligações “sigma”, não impedindo que átomos maiores formem ligações múltiplas.
( ) Os diagramas de níveis de energia de orbitais moleculares de moléculas diatômicas heteronucleares são fáceis de predizer qualitativamente. Entretanto, são dificilmente calculados usando softwares específicos disponíveis.
( ) Na Teoria dos Orbitais Moleculares, todos os elétrons de valência estão deslocalizados sobre toda a molécula, isto é, não pertencem a alguma ligação específica.
A ordem correta de preenchimento dos parênteses, de cima para baixo, é:
( ) A teoria dos orbitais moleculares é a que melhor descreve a ligação química, pois resolve as deficiências da Teoria de Lewis e é mais simples na utilização dos cálculos quando comparada à Teoria de Valência.
( ) Nas ligações múltiplas, um átomo forma uma ligação “sigma” usando um orbital híbrido (sp ou sp2 ) e uma ou mais ligações “pi” usando orbitais não hibridados. A superposição lateral que produz uma ligação “pi” não restringe a rotação das moléculas, resultando em ligações mais fracas do que as ligações “sigma”, não impedindo que átomos maiores formem ligações múltiplas.
( ) Os diagramas de níveis de energia de orbitais moleculares de moléculas diatômicas heteronucleares são fáceis de predizer qualitativamente. Entretanto, são dificilmente calculados usando softwares específicos disponíveis.
( ) Na Teoria dos Orbitais Moleculares, todos os elétrons de valência estão deslocalizados sobre toda a molécula, isto é, não pertencem a alguma ligação específica.
A ordem correta de preenchimento dos parênteses, de cima para baixo, é:
Q2358165
Química
A Tabela Periódica pode ser usada na predição de inúmeras propriedades, muitas das
quais são cruciais para a compreensão da Química. Em relação à classificação periódica dos elementos
e propriedades periódicas, assinale a alternativa INCORRETA.
Q2358166
Química
Quanto à isomeria plana apresentada pelos compostos abaixo, relacione a Coluna 1
à Coluna 2.
Coluna 1
1. Etanol e metoximetano.
2. Ciclopropano e propeno.
3. Butan-2-ol e butan-1-ol.
4. Metanoato de etila e etanoato de etila. 5. Etanal e etenol.
Coluna 2
( ) Isomeria de posição.
( ) Isomeria de compensação ou metameria.
( ) Isomeria de função.
( ) Isomeria dinâmica ou tautomeria.
( ) Isomeria de cadeia.
A ordem correta de preenchimento dos parênteses, de cima para baixo, é:
Coluna 1
1. Etanol e metoximetano.
2. Ciclopropano e propeno.
3. Butan-2-ol e butan-1-ol.
4. Metanoato de etila e etanoato de etila. 5. Etanal e etenol.
Coluna 2
( ) Isomeria de posição.
( ) Isomeria de compensação ou metameria.
( ) Isomeria de função.
( ) Isomeria dinâmica ou tautomeria.
( ) Isomeria de cadeia.
A ordem correta de preenchimento dos parênteses, de cima para baixo, é:
Q2358167
Química
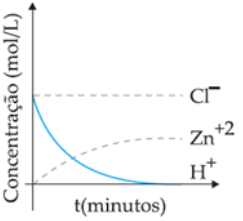
O gráfico a seguir representa a variação de concentração com o tempo durante a
reação de ácido clorídrico com zinco metálico. Analise-o e assinale a alternativa correta.

Q2358168
Química
O álcool amílico, C5H11OH, apresenta a reação de combustão a seguir:
C5H11OH + O2 → CO2 + H2O
Com base nessa equação, assinale a alternativa correta.
C5H11OH + O2 → CO2 + H2O
Com base nessa equação, assinale a alternativa correta.