Questões de Concurso Comentadas sobre química para seduc-pe
Foram encontradas 6 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Q701280
Química
Em um laboratório foi montada uma aparelhagem para
recolhimento do gás oxigênio produzido na reação de
decomposição do clorato de potássio, como ilustra a figura a
seguir.
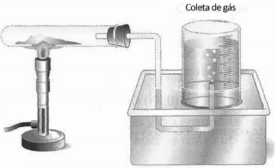
A reação observada pode ser representada pela equação: 2 KClO3 → 2 KCl + 3 O2 Uma amostra de clorato de potássio foi parcialmente decomposta sendo a pressão do gás recolhido de 0,8 atm e seu volume de 180 mL na temperatura de 27ºC. Considerando o comportamento ideal do gás, a massa de clorato de potássio que sofreu decomposição foi de, aproximadamente, Dados: Massa Molar: KClO3 = 122,5 g.mol-1 Constante real dos gases R= 0,082atm.L.mol-1 .K-1

A reação observada pode ser representada pela equação: 2 KClO3 → 2 KCl + 3 O2 Uma amostra de clorato de potássio foi parcialmente decomposta sendo a pressão do gás recolhido de 0,8 atm e seu volume de 180 mL na temperatura de 27ºC. Considerando o comportamento ideal do gás, a massa de clorato de potássio que sofreu decomposição foi de, aproximadamente, Dados: Massa Molar: KClO3 = 122,5 g.mol-1 Constante real dos gases R= 0,082atm.L.mol-1 .K-1
Q701278
Química
O ácido benzoico foi descoberto no século XVI e recebeu esse
nome por ter sido extraído do benjoeiro.
Em 1875, Salkowski verificou que esse ácido atua como fungicida
e, desde então, o ácido benzoico vem sendo usado como
germicida na preservação de alimentos e como adjuvante
farmacológico anti-fúngico, normalmente em concentrações que
variam entre 0,05 a 0,15%. Trata-se de um composto de fórmula
molecular C7H6O2
(massa molar = 122 g.mol -1
) pouco solúvel em
água.
Em uma solução aquosa, comporta-se como um ácido fraco, com
pKa = 4.
Uma solução aquosa de ácido benzoico em concentração 0,12%
(m/v) apresenta pH aproximadamente igual a
Q701274
Química
Uma técnica usada em laboratórios químicos é a determinação
das fórmulas empíricas (mínimas) pela análise por combustão.
Nesse processo, queima-se uma amostra em um tubo por onde
passa um fluxo abundante de oxigênio, sendo todo o hidrogênio
do composto convertido em água e todo o carbono convertido
em dióxido de carbono.
O equipamento utilizado é representado pela figura a seguir.
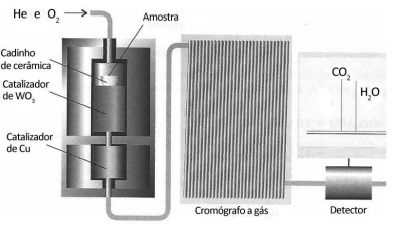
Na análise por combustão de 6,0 g de um hidrocarboneto recém-sintetizado foi determinada a massa de 17,6 g de dióxido de carbono e 10,8 g de água. A fórmula empírica desse composto é: Dados: Massas Molares: H = 1g.mol–1 C = 12g.mol–1 O=16g.mol–1

Na análise por combustão de 6,0 g de um hidrocarboneto recém-sintetizado foi determinada a massa de 17,6 g de dióxido de carbono e 10,8 g de água. A fórmula empírica desse composto é: Dados: Massas Molares: H = 1g.mol–1 C = 12g.mol–1 O=16g.mol–1
Q701272
Química
Na determinação do teor de acidez de uma amostra de suco de
laranja comercial, 10,00 mL de amostra foram levados para
erlenmeyer. Adicionou-se água destilada até completar cerca de
50 mL, 3 gotas de fenolftaleína e titulou-se contra solução padrão
de NaOH até mudança de coloração. Na titulação, foram gastos
3,90 mL de solução padrão 0,100 mol.L–1
.
A acidez é expressa em termos do teor (porcentagem
massa/volume) de ácido cítrico, cuja fórmula estrutural é
apresentada a seguir.
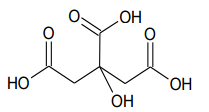
Assinale a opção que expressa a acidez da amostra. Dados. Massa molar. Ácido Cítrico: 192 g.mol –1 .

Assinale a opção que expressa a acidez da amostra. Dados. Massa molar. Ácido Cítrico: 192 g.mol –1 .
Q701265
Química
Para a determinação da pureza do sal sulfato de potássio, 0,500 g
de amostra foram tratadas com excesso de solução de cloreto de
bário. O precipitado obtido foi lavado, seco e calcinado a 500ºC
até peso constante. A massa final do precipitado foi 0,466 g.
A pureza da amostra em termos de sulfato de potássio é
de, aproximadamente,
Dados: Massas molares (g.mol –1
) K2SO4: 174; KCl: 74,5; BaSO4: 233