Questões de Vestibular de Química - Eletroquímica: Oxirredução, Potenciais Padrão de Redução, Pilha, Eletrólise e Leis de Faraday.
Foram encontradas 417 questões
Ano: 2019
Banca:
Instituto Consulplan
Órgão:
FIMCA
Prova:
Instituto Consulplan - 2019 - FIMCA - Vestibular de Medicina - Edital nº 01/ 2020 |
Q1790455
Química
Considerando o estudo da eletrólise ígnea do cloreto de
magnésio, indique a quantidade de massa de magnésio
metálico obtido quando uma corrente de 10 A atravessa a
cuba eletrolítica durante 40 minutos.
Ano: 2019
Banca:
Instituto Consulplan
Órgão:
FASEH
Provas:
Instituto Consulplan - 2019 - FASEH - Vestibular de Medicina - Tipo 01
|
Instituto Consulplan - 2019 - FASEH - Vestibular de Medicina |
Q1785770
Química
Uma das modalidades de energia de grande importância
em nossa vida é a energia elétrica. A eletroquímica é a
parte da química que estuda não só os fenômenos
envolvidos na produção de corrente elétrica a partir da
transferência de elétrons, mas também a utilização de
corrente elétrica na produção dessas reações. Considere
uma pilha de cobre e prata e os seus dados:
Ered(Ag+/Ag) = 0,80 v Ered(Cu2+/Cu) = 0,34 v
O cátodo, o ânodo e o valor de ∆E0 , respectivamente, da pilha são:
Ered(Ag+/Ag) = 0,80 v Ered(Cu2+/Cu) = 0,34 v
O cátodo, o ânodo e o valor de ∆E0 , respectivamente, da pilha são:
Ano: 2019
Banca:
UFRGS
Órgão:
UFRGS
Prova:
UFRGS - 2019 - UFRGS - Vestibular - UFRGS - Biologia, Química e Geografia |
Q1784293
Química
Baterias de Li - CO2 são de grande interesse atual, devido a questões ambientais e energéticas, pois
utilizam CO2 e abrem um novo caminho para conversão e armazenamento de energia. Uma das propostas sobre as semirreações eletroquímicas envolvidas nessa bateria é apresentada
abaixo.
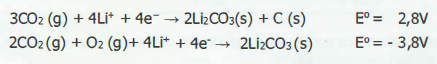
Sobre essas baterias, é correto afirmar que
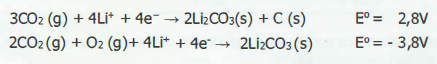
Sobre essas baterias, é correto afirmar que
Q1783362
Química
O escurecimento de talheres de prata pode ocorrer devido à presença de derivados de enxofre encontrados nos
alimentos. A equação química de oxidação e redução que representa esse processo está descrita a seguir.
4Ag(s) + 2H2S(g) + O2(g) 2Ag2S(s) + 2H2O(l)
2Ag2S(s) + 2H2O(l)
Nesse processo, o agente redutor é
4Ag(s) + 2H2S(g) + O2(g)
 2Ag2S(s) + 2H2O(l)
2Ag2S(s) + 2H2O(l)
Nesse processo, o agente redutor é
Q1712820
Química
Analise a tabela de potenciais padrão de redução a
seguir:
Semirreação Eu (V) Al3+ (aq) + 3 e- ⇌ A I (s) -1,66 Zn2+ (aq) + 2 e- ⇌ Zn (s) -0,76 Fe2+ (aq) + 2 e- ⇌ Fe (s) -0,44 Cu2+ (aq) + 2 e- ⇌ Cu (s) +0,34 Ag+ (aq) + e- ⇌ A g (s) +0,80
Com base na tabela, a afirmativa correta em relação ao processo de corrosão de metais é:
Semirreação Eu (V) Al3+ (aq) + 3 e- ⇌ A I (s) -1,66 Zn2+ (aq) + 2 e- ⇌ Zn (s) -0,76 Fe2+ (aq) + 2 e- ⇌ Fe (s) -0,44 Cu2+ (aq) + 2 e- ⇌ Cu (s) +0,34 Ag+ (aq) + e- ⇌ A g (s) +0,80
Com base na tabela, a afirmativa correta em relação ao processo de corrosão de metais é:
