Questões de Vestibular de Química - Velocidade de Reação, Energia de Ativação, Concentração, Pressão, Temperatura e Catalisador
Foram encontradas 51 questões
Ano: 2011
Banca:
UECE-CEV
Órgão:
UECE
Prova:
UECE-CEV - 2011 - UECE - Vestibular - Física e Química 01 |
Q238129
Química
A queima de combustíveis fósseis nos veículos automotores produz uma infinidade de substâncias causadoras do efeito estufa, da chuva ácida e de danos irreparáveis aos ciclos biogeoquímicos do planeta. Contudo, esses efeitos podem ser minimizados por catálise. Sobre catálise e conversores catalíticos automotivos leia as frases abaixo, assinale com V, as verdadeiras e com F, as falsas.
( ) O processo que ocorre no cano de descarga dos veículos automotivos é uma catálise homogênea.
( ) Óxidos de nitrogênio, oriundos das descargas dos veículos, são responsáveis pela névoa fotoquímica.
( ) O conversor catalítico oxida o CO e hidrocarbonetos não queimados, transformando-os em dióxido de carbono e água.
( ) O conversor catalítico reduz os óxidos de nitrogênio a nitrogênio gasoso.
( ) Os conversores catalíticos eliminam totalmente a poluição atmosférica causada pelos gases liberados na descarga dos veículos automotivos.
A sequência correta, de cima para baixo, é
( ) O processo que ocorre no cano de descarga dos veículos automotivos é uma catálise homogênea.
( ) Óxidos de nitrogênio, oriundos das descargas dos veículos, são responsáveis pela névoa fotoquímica.
( ) O conversor catalítico oxida o CO e hidrocarbonetos não queimados, transformando-os em dióxido de carbono e água.
( ) O conversor catalítico reduz os óxidos de nitrogênio a nitrogênio gasoso.
( ) Os conversores catalíticos eliminam totalmente a poluição atmosférica causada pelos gases liberados na descarga dos veículos automotivos.
A sequência correta, de cima para baixo, é
Ano: 2011
Banca:
UECE-CEV
Órgão:
UECE
Prova:
UECE-CEV - 2011 - UECE - Vestibular - Física e Química 01 |
Q238122
Química
A imprensa registra com muita insistência o processo de degradação das colunas do Parthenon grego e de outros monumentos em consequência da poluição ambiental. A reação a seguir mostra como acontece o ataque aos monumentos de mármore: 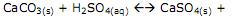
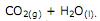 A reação se torna mais agressiva por sofrer um natural deslocamento para a direita. Apenas com as informações disponíveis na equação acima, marque a alternativa que contempla a explicação para esse fato.
A reação se torna mais agressiva por sofrer um natural deslocamento para a direita. Apenas com as informações disponíveis na equação acima, marque a alternativa que contempla a explicação para esse fato.
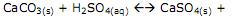
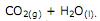 A reação se torna mais agressiva por sofrer um natural deslocamento para a direita. Apenas com as informações disponíveis na equação acima, marque a alternativa que contempla a explicação para esse fato.
A reação se torna mais agressiva por sofrer um natural deslocamento para a direita. Apenas com as informações disponíveis na equação acima, marque a alternativa que contempla a explicação para esse fato.
Q230010
Química
Texto associado
Leia atentamente o texto IV e responda às questões de 09 a 11.


Julgue os itens a seguir, de acordo com as informações dadas no texto IV e seus conhecimentos sobre química:
I. Na reação de hidrogenação da quinona temos cetonas sendo convertidas em fenóis pela quebra da ligação C=O, seguida da adição de hidrogênio. Tanto o carbono quanto o oxigênio de cada carbonila recebem um átomo de hidrogênio.
II. Na reação de oxidação temos um álcool sendo convertido em um aldeído, e a água é um dos produtos dessa reação.
III. A quinona participa do processo de obtenção do Peróxido de Hidrogênio como uma substância catalisadora, podendo ser recuperada para a produção de mais H2 O2 .
IV. O peróxido de hidrogênio (H2 O2 ) é uma substância letal aos humanos, mesmo em pequenas quantidades.
Está(ão) correta(s) a(s) alternativa(s):
I. Na reação de hidrogenação da quinona temos cetonas sendo convertidas em fenóis pela quebra da ligação C=O, seguida da adição de hidrogênio. Tanto o carbono quanto o oxigênio de cada carbonila recebem um átomo de hidrogênio.
II. Na reação de oxidação temos um álcool sendo convertido em um aldeído, e a água é um dos produtos dessa reação.
III. A quinona participa do processo de obtenção do Peróxido de Hidrogênio como uma substância catalisadora, podendo ser recuperada para a produção de mais H2 O2 .
IV. O peróxido de hidrogênio (H2 O2 ) é uma substância letal aos humanos, mesmo em pequenas quantidades.
Está(ão) correta(s) a(s) alternativa(s):
Q229351
Química
Julgue os itens que seguem:
I - No instante t = 60 s, a velocidade da produção do gás hidrogênio é maior que a velocidade de consumo de Mg (em mols/s).
II - Em qualquer instante após o início da reação, a quantidade de matéria (mol) produzida de gás hidrogênio é o dobro da consumida de ácido clorídrico.
III - A massa de gás hidrogênio produzida é sempre menor que a massa de ácido consumida, em qualquer instante.
Está(ão) correto(s):
I - No instante t = 60 s, a velocidade da produção do gás hidrogênio é maior que a velocidade de consumo de Mg (em mols/s).
II - Em qualquer instante após o início da reação, a quantidade de matéria (mol) produzida de gás hidrogênio é o dobro da consumida de ácido clorídrico.
III - A massa de gás hidrogênio produzida é sempre menor que a massa de ácido consumida, em qualquer instante.
Está(ão) correto(s):
Q226053
Química
A reação do eteno, C2H4 com hidrogênio, H2 produz etano, C2H6.
Sabe-se que, no equilíbrio, a velocidade de formação dos produtos, V, e a velocidade inversa, de formação dos reagentes, V’ , são iguais:

Foram realizados dois experimentos envolvendo essa reação, com apenas uma diferença: um, na presença de catalisador; o outro, na ausência deste.
Comparando-se esses dois experimentos, é CORRETO afirmar que, na reação catalisada, aumenta
Sabe-se que, no equilíbrio, a velocidade de formação dos produtos, V, e a velocidade inversa, de formação dos reagentes, V’ , são iguais:

Foram realizados dois experimentos envolvendo essa reação, com apenas uma diferença: um, na presença de catalisador; o outro, na ausência deste.
Comparando-se esses dois experimentos, é CORRETO afirmar que, na reação catalisada, aumenta
