Questões de Vestibular CESMAC 2015 para Prova Medicina-2016.1- 2° DIA- PROVA TIPO 1
Foram encontradas 4 questões
Ano: 2015
Banca:
Cepros
Órgão:
CESMAC
Prova:
Cepros - 2015 - CESMAC - Prova Medicina-2016.1- 2° DIA- PROVA TIPO 1 |
Q1344910
Química
A química nuclear transformou os diagnósticos
médicos. Os traçadores radioativos são utilizados para
medir as funções de diferentes órgãos do corpo
humano. Por exemplo, o isótopo sódio-24 (2411Na) é
usado para monitorar o fluxo sanguíneo. Sabendo que
o nuclídeo 2411Na se desintegra, espontaneamente,
originando o nuclídeo 2412Mg , de acordo com a
equação:
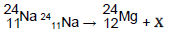
para completar a equação dessa reação nuclear, a espécie X deve ser:
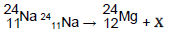
para completar a equação dessa reação nuclear, a espécie X deve ser:
Ano: 2015
Banca:
Cepros
Órgão:
CESMAC
Prova:
Cepros - 2015 - CESMAC - Prova Medicina-2016.1- 2° DIA- PROVA TIPO 1 |
Q1344919
Química
A propulsão de um ônibus espacial ocorre através da
reação do hidrogênio com oxigênio. Os tanques
desses combustíveis são externos e separados,
carregando 1,20 x 106
L de hidrogênio líquido a -253ºC
e 0,55 x 106
L de oxigênio líquido a -183ºC. Nessas
temperaturas, a densidade do hidrogênio é 34 mol.L-1
e a do oxigênio é 37 mol.L-1.
H2(l) + ½ O2(l) → H2O(g), ∆H = -242 kJ.mol-1
Levando-se em consideração a aplicação, e que todo o combustível é consumido, qual é a energia (J) liberada para propulsão do ônibus espacial?
H2(l) + ½ O2(l) → H2O(g), ∆H = -242 kJ.mol-1
Levando-se em consideração a aplicação, e que todo o combustível é consumido, qual é a energia (J) liberada para propulsão do ônibus espacial?
Ano: 2015
Banca:
Cepros
Órgão:
CESMAC
Prova:
Cepros - 2015 - CESMAC - Prova Medicina-2016.1- 2° DIA- PROVA TIPO 1 |
Q1344922
Química
A maior parte da energia de nossos corpos provem de
carboidratos e gorduras. Os carboidratos se
decompõem em glicose, C6H12O6, no intestino.
Transportada pelo sangue, a glicose chega às células,
onde reage com o oxigênio numa sequência de
reações que levam à produção final de gás CO2, água
líquida e energia:
C6H12O6(s) + 6 O2 (g) → 6 CO2(g) + 6 H2O(l)
Calcule a entalpia padrão de combustão da glicose sabendo as entalpias padrão de formação:
∆Hf°(C6H12O6,s) = −1.268 kJ∙mol−1 ∆Hf°(CO2,g) = −393,51 kJ∙mol−1 ∆Hf°(H2O,l) = −285,83 kJ∙mol−1
C6H12O6(s) + 6 O2 (g) → 6 CO2(g) + 6 H2O(l)
Calcule a entalpia padrão de combustão da glicose sabendo as entalpias padrão de formação:
∆Hf°(C6H12O6,s) = −1.268 kJ∙mol−1 ∆Hf°(CO2,g) = −393,51 kJ∙mol−1 ∆Hf°(H2O,l) = −285,83 kJ∙mol−1
Ano: 2015
Banca:
Cepros
Órgão:
CESMAC
Prova:
Cepros - 2015 - CESMAC - Prova Medicina-2016.1- 2° DIA- PROVA TIPO 1 |
Q1344923
Química
O tipo de pilha mais utilizado em equipamentos
eletrônicos são as pilhas alcalinas. Elas são chamadas
de alcalinas por causa do tipo de eletrólito utilizado
(KOH). As reações que ocorrem em uma pilha alcalina
estão descritas nas equações abaixo.
I. Zn(s) + 2OH− (aq) → ZnO(s) + H2O(l) + 2e− , E° = +1,26 V
II. 2MnO2(s) + H2O(l) + 2e− → Mn2O3(s) + 2OH− (aq), E° = +0,26 V
É correto afirmar sobre as pilhas alcalinas:
1) A reação (I) ocorre no ânodo; a reação (II) ocorre no cátodo.
2) A concentração do eletrólito alcalino (KOH) é mantida constante.
3) O potencial de cela (∆E°) desenvolvido através da célula eletroquímica, envolvendo as duas reações (I e II), será de +1,52 V.
Está(ão) correta(s) a(s) afirmativa(s):
I. Zn(s) + 2OH− (aq) → ZnO(s) + H2O(l) + 2e− , E° = +1,26 V
II. 2MnO2(s) + H2O(l) + 2e− → Mn2O3(s) + 2OH− (aq), E° = +0,26 V
É correto afirmar sobre as pilhas alcalinas:
1) A reação (I) ocorre no ânodo; a reação (II) ocorre no cátodo.
2) A concentração do eletrólito alcalino (KOH) é mantida constante.
3) O potencial de cela (∆E°) desenvolvido através da célula eletroquímica, envolvendo as duas reações (I e II), será de +1,52 V.
Está(ão) correta(s) a(s) afirmativa(s):