Questões de Vestibular UEFS 2009 para Vestibular, Física, Química e Biologia
Foram encontradas 20 questões
Ano: 2009
Banca:
UEFS
Órgão:
UEFS
Prova:
UEFS - 2009 - UEFS - Vestibular - Física, Química e Biologia |
Q1372632
Química
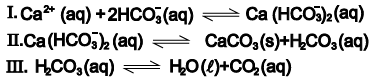
As algas zooxanthellae são também responsáveis pela intensa precipitação de carbonatos no esqueleto dos corais escleractíneos principais formadores dos recifes. Em pH próximo a 8,5, a maior parte do CO2 (aq) disponível na água do mar se encontra na forma de íons bicarbonato, HCO3- (aq). Devido à intensa radiação solar, os corais e os invertebrados que possuem algas simbiontes — sensíveis a pequenas alterações de temperatura — capturam ativamente íons de cálcio, Ca2+(aq), que reagem com íons bicarbonato.O bicarbonato de cálcio se decompõe em carbonato de cálcio, que se precipita sob forma de esqueleto, e ácido carbônico, H2CO3 (aq), usado na fotossíntese. Trata-se de um processo bioquímico muito eficiente, porém sujeito às alterações das concentrações de CO2 (g), na atmosfera.
Uma análise do processo bioquímico de formação de esqueleto de carbonato de cálcio dos corais escleractíneos referidos no texto e de acordo com as equações químicas I, II e III, permite afirmar:
Ano: 2009
Banca:
UEFS
Órgão:
UEFS
Prova:
UEFS - 2009 - UEFS - Vestibular - Física, Química e Biologia |
Q1372633
Química
O ácido nítrico é importante matéria-prima para a produção de explosivos, fertilizantes e corantes de
tecidos. É obtido industrialmente a partir da reação de amônia com o oxigênio, na presença de
catalisador de platina, de acordo com as equações químicas que representam, resumidamente, esse
processo
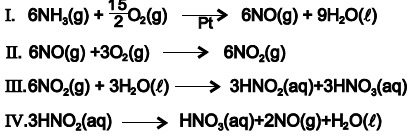
Com base nessas informações e de acordo com as equações químicas que representam o processo de fabricação do ácido nítrico, é correto afirmar:

Com base nessas informações e de acordo com as equações químicas que representam o processo de fabricação do ácido nítrico, é correto afirmar:
Ano: 2009
Banca:
UEFS
Órgão:
UEFS
Prova:
UEFS - 2009 - UEFS - Vestibular - Física, Química e Biologia |
Q1372634
Química
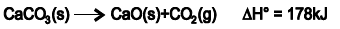
O calcário formado principalmente por carbonato de cálcio, CaCO3 (s), é um mineral importante na correção da acidez do solo, na produção de cimento e de óxido de cálcio CaO, conhecido como cal.
O Brasil utiliza cerca de um milhão de toneladas de óxido de cálcio por ano. A partir da decomposição térmica do carbonato de cálcio representada pela equação química, é correto afirmar:
Ano: 2009
Banca:
UEFS
Órgão:
UEFS
Prova:
UEFS - 2009 - UEFS - Vestibular - Física, Química e Biologia |
Q1372635
Química
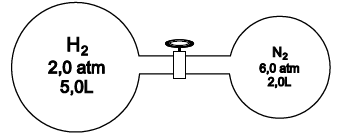
A figura representa um sistema formado por dois recipientes interligados por uma válvula fechada, a determinada temperatura, contendo, respectivamente, os gases ideais, hélio e nitrogênio, nas condições apresentadas.
A partir da abertura da válvula, a essa temperatura, é correto afirmar:
Ano: 2009
Banca:
UEFS
Órgão:
UEFS
Prova:
UEFS - 2009 - UEFS - Vestibular - Física, Química e Biologia |
Q1372636
Química
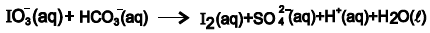
O iodato de sódio, NaIO3 , é utilizado como aditivo de sal de cozinha, NaCl, com objetivo de prevenir o bócio, uma doença provocada pela deficiência de iodo na alimentação. A equação química não balanceada representa a reação do íon iodato com o íon hidrogeno-sulfito, na determinação de iodo, I2 .
A partir do balanceamento da equação química com os menores coeficientes estequiométricos inteiros, é correto afirmar: