Questões de Vestibular UEM 2011 para Vestibular - PAS - Etapa 2 - Francês
Foram encontradas 9 questões
Ano: 2011
Banca:
UEM
Órgão:
UEM
Provas:
UEM - 2011 - UEM - Vestibular - PAS - Etapa 2 - Inglês
|
UEM - 2011 - UEM - Vestibular - PAS - Etapa 2 - Francês |
Q1349926
Química
Texto associado
O gás amônia (NH3) em contato com água sofre a
seguinte reação química, formando hidróxido de
amônio:
NH3(g) + H2O(I)  NH4OH(aq)
NH4OH(aq)  NH+4 (aq) + OH− (aq)
NH+4 (aq) + OH− (aq)
 NH4OH(aq)
NH4OH(aq)  NH+4 (aq) + OH− (aq)
NH+4 (aq) + OH− (aq)
De acordo com essa informação, assinale o que for
correto.
O hidróxido de amônio é uma dibase.
Ano: 2011
Banca:
UEM
Órgão:
UEM
Provas:
UEM - 2011 - UEM - Vestibular - PAS - Etapa 2 - Inglês
|
UEM - 2011 - UEM - Vestibular - PAS - Etapa 2 - Francês |
Q1349928
Química
Texto associado
O gás amônia (NH3) em contato com água sofre a
seguinte reação química, formando hidróxido de
amônio:
NH3(g) + H2O(I)  NH4OH(aq)
NH4OH(aq)  NH+4 (aq) + OH− (aq)
NH+4 (aq) + OH− (aq)
 NH4OH(aq)
NH4OH(aq)  NH+4 (aq) + OH− (aq)
NH+4 (aq) + OH− (aq)
De acordo com essa informação, assinale o que for
correto.
O hidróxido de amônio é uma base forte.
Ano: 2011
Banca:
UEM
Órgão:
UEM
Provas:
UEM - 2011 - UEM - Vestibular - PAS - Etapa 2 - Inglês
|
UEM - 2011 - UEM - Vestibular - PAS - Etapa 2 - Francês |
Q1349929
Química
Texto associado
O gás amônia (NH3) em contato com água sofre a
seguinte reação química, formando hidróxido de
amônio:
NH3(g) + H2O(I)  NH4OH(aq)
NH4OH(aq)  NH+4 (aq) + OH− (aq)
NH+4 (aq) + OH− (aq)
 NH4OH(aq)
NH4OH(aq)  NH+4 (aq) + OH− (aq)
NH+4 (aq) + OH− (aq)
De acordo com essa informação, assinale o que for
correto.
Para ser utilizado pelas células vegetais, o
nitrogênio precisa estar na forma de íons
amônio (NH+4) ou de íons nitrato (NO−3) .
Ano: 2011
Banca:
UEM
Órgão:
UEM
Provas:
UEM - 2011 - UEM - Vestibular - PAS - Etapa 2 - Inglês
|
UEM - 2011 - UEM - Vestibular - PAS - Etapa 2 - Francês |
Q1349946
Química
Texto associado
A principal substância orgânica nitrogenada
excretada pelas aves é o ácido úrico, removido do
sangue pelos rins e conduzido à cloaca pelos
ureteres. Na cloaca, o ácido úrico, altamente
concentrado, adquire cor esbranquiçada e
consistência pastosa e, posteriormente, é eliminado
juntamente com as fezes. O sangue humano
também contém ácido úrico, cuja concentração,
normalmente, varia entre 3,5 e 7,2 mg/dL.
Considerando que a massa molar do ácido úrico é
168,0 g/mol, assinale o que for correto.
No sangue humano, uma concentração de
ácido úrico no valor de 4,5 x 10– 4 mol/dL, está
fora da faixa de normalidade.
Ano: 2011
Banca:
UEM
Órgão:
UEM
Provas:
UEM - 2011 - UEM - Vestibular - PAS - Etapa 2 - Inglês
|
UEM - 2011 - UEM - Vestibular - PAS - Etapa 2 - Francês |
Q1349961
Química
Texto associado
Ao preparar uma solução de Ca(NO3)2 (nitrato de cálcio) em laboratório, um aluno, inadvertidamente, pesou 1,64 g de NH4NO3 (nitrato de amônio) por engano e o dissolveu em água destilada, preparando 1,0 L de solução. Considerando a densidade da água igual a 1,0 g/mL a 25 °C, e dadas as massas molares dos sais,
Ca(NO3)2 = 164 g/mol
CLASSIFICAÇÃO PERIÓDICA DOS ELEMENTOS
COM MASSAS ATÔMICAS REFERIDAS AO ISÓTOPO 12 DO CARBONO
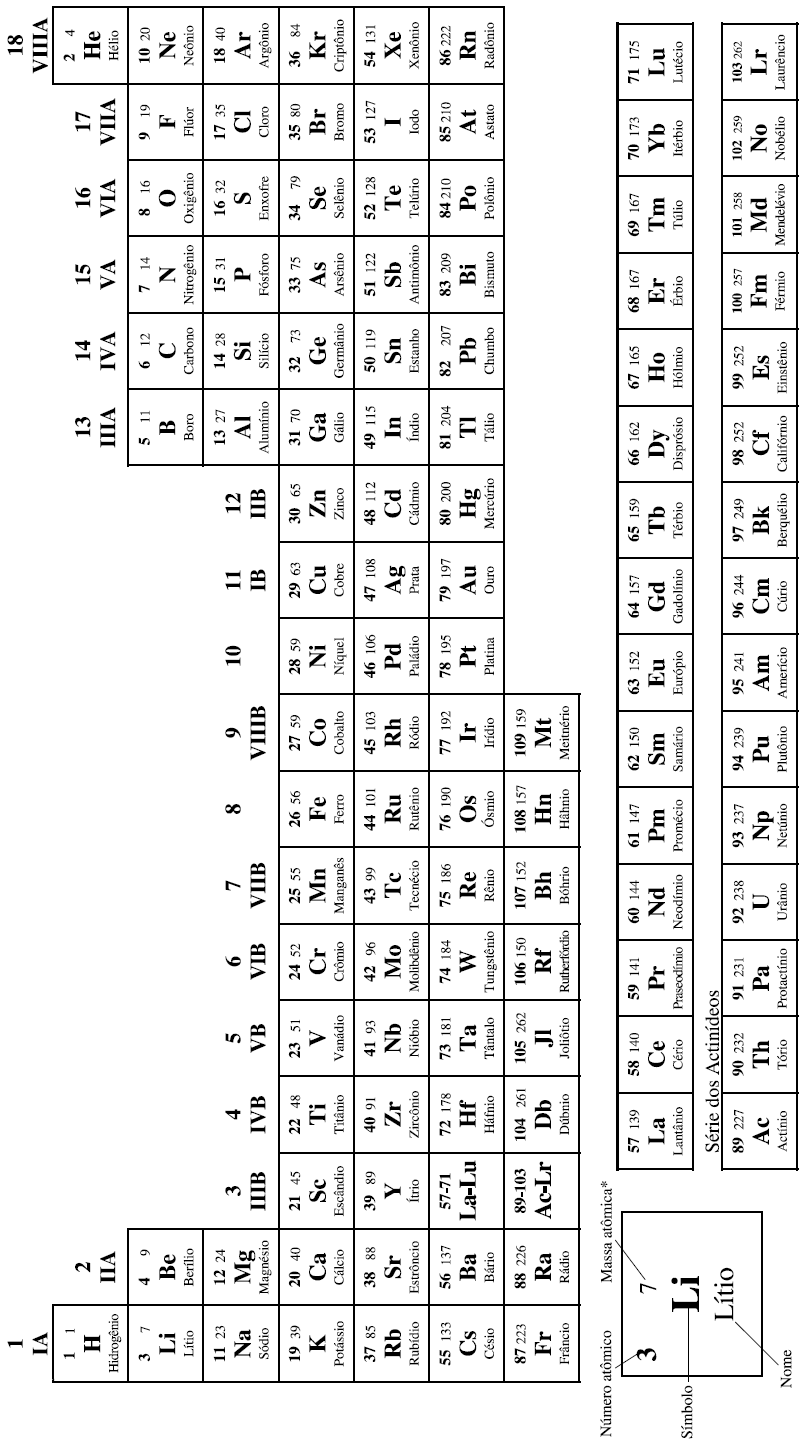
*OS VALORES DAS MASSAS ATÔMICAS DOS ELEMENTOS FORAM ARREDONDADAS PARA FACILITAR OS CÁLCULOS. ESTA TABELA PERIÓDICA É EXCLUSIVA PARA ESTE PROCESSO E NÃO DEVE SER UTILIZADA PARA OUTRAS FINALIDADES.
COM MASSAS ATÔMICAS REFERIDAS AO ISÓTOPO 12 DO CARBONO

*OS VALORES DAS MASSAS ATÔMICAS DOS ELEMENTOS FORAM ARREDONDADAS PARA FACILITAR OS CÁLCULOS. ESTA TABELA PERIÓDICA É EXCLUSIVA PARA ESTE PROCESSO E NÃO DEVE SER UTILIZADA PARA OUTRAS FINALIDADES.
Ao preparar uma solução de Ca(NO3)2 (nitrato de cálcio) em laboratório, um aluno, inadvertidamente, pesou 1,64 g de NH4NO3 (nitrato de amônio) por engano e o dissolveu em água destilada, preparando 1,0 L de solução. Considerando a densidade da água igual a 1,0 g/mL a 25 °C, e dadas as massas molares dos sais,
Ca(NO3)2 = 164 g/mol
NH4NO3 = 80 g/mol, assinale a alternativa correta.
A temperatura de ebulição da solução de
NH4NO3 é maior que a temperatura de ebulição
da solução de Ca(NO3)2, considerando a
mesma massa dos dois sais (1,64 g)
dissolvidas em 1,0 L de solução.