Questões de Vestibular UERJ 2013 para Vestibular, Segundo Exame - Espanhol
Foram encontradas 4 questões
Ano: 2013
Banca:
UERJ
Órgão:
UERJ
Provas:
UERJ - 2013 - UERJ - Vestibular - Segundo Exame
|
UERJ - 2013 - UERJ - Vestibular - Segundo Exame - Francês |
UERJ - 2013 - UERJ - Vestibular - Segundo Exame - Espanhol |
Q581320
Química
Um nanotubo é uma estrutura cilíndrica microscópica formada apenas por átomos de carbono
com hibridação sp2
.
O esquema abaixo representa um corte lateral de um nanotubo. Cada esfera corresponde ao núcleo de um átomo e cada traço a uma ligação entre carbonos. Não estão indicadas no esquema as ligações do tipo pi.
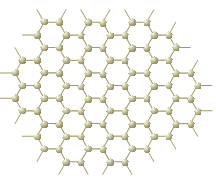
O número de ligações duplas realizadas por átomo em um nanotubo corresponde a:
O esquema abaixo representa um corte lateral de um nanotubo. Cada esfera corresponde ao núcleo de um átomo e cada traço a uma ligação entre carbonos. Não estão indicadas no esquema as ligações do tipo pi.

O número de ligações duplas realizadas por átomo em um nanotubo corresponde a:
Ano: 2013
Banca:
UERJ
Órgão:
UERJ
Provas:
UERJ - 2013 - UERJ - Vestibular - Segundo Exame
|
UERJ - 2013 - UERJ - Vestibular - Segundo Exame - Francês |
UERJ - 2013 - UERJ - Vestibular - Segundo Exame - Espanhol |
Q581324
Química
Uma forma de identificar a estabilidade de um átomo de qualquer elemento químico consiste
em relacionar seu número de prótons com seu número de nêutrons em um gráfico denominado
diagrama de estabilidade, mostrado a seguir.
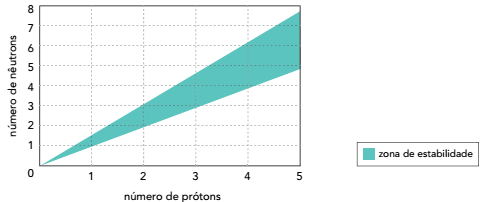
São considerados estáveis os átomos cuja interseção entre o número de prótons e o de nêutrons se encontra dentro da zona de estabilidade mostrada no gráfico.
Verifica-se, com base no diagrama, que o menor número de massa de um isótopo estável de um metal é igual a:

São considerados estáveis os átomos cuja interseção entre o número de prótons e o de nêutrons se encontra dentro da zona de estabilidade mostrada no gráfico.
Verifica-se, com base no diagrama, que o menor número de massa de um isótopo estável de um metal é igual a:
Ano: 2013
Banca:
UERJ
Órgão:
UERJ
Provas:
UERJ - 2013 - UERJ - Vestibular - Segundo Exame
|
UERJ - 2013 - UERJ - Vestibular - Segundo Exame - Francês |
UERJ - 2013 - UERJ - Vestibular - Segundo Exame - Espanhol |
Q581328
Química
Uma das técnicas empregadas para separar uma mistura gasosa de CO2
e CH4
consiste em fazê-la
passar por uma solução aquosa de Ba(OH)2
.
Uma amostra dessa mistura gasosa, com volume total de 30 L, sob temperatura de 27 ºC e pressão de 1 atm, ao reagir com a solução aquosa de Ba(OH)2 , produz a precipitação de 98,5 g de BaCO3 . A fração gasosa remanescente, nas mesmas condições de temperatura e pressão, contém apenas CH4 .
Uma amostra dessa mistura gasosa, com volume total de 30 L, sob temperatura de 27 ºC e pressão de 1 atm, ao reagir com a solução aquosa de Ba(OH)2 , produz a precipitação de 98,5 g de BaCO3 . A fração gasosa remanescente, nas mesmas condições de temperatura e pressão, contém apenas CH4 .
Ano: 2013
Banca:
UERJ
Órgão:
UERJ
Provas:
UERJ - 2013 - UERJ - Vestibular - Segundo Exame - Francês
|
UERJ - 2013 - UERJ - Vestibular - Segundo Exame - Espanhol |
Q1283579
Química
Texto associado
Com as chuvas intensas que caíram na cidade do Rio de Janeiro em março de 2013, grande
quantidade de matéria orgânica se depositou na lagoa Rodrigo de Freitas. O consumo biológico
desse material contribuiu para a redução a zero do nível de gás oxigênio dissolvido na água,
provocando a mortandade dos peixes.
O volume médio de água na lagoa é igual a 6,2 x 106
L. Imediatamente antes de ocorrer a
mortandade dos peixes, a concentração de gás oxigênio dissolvido na água correspondia
a 2,5 x 10-4
mol.L-1
.
Ao final da mortandade, a quantidade consumida, em quilogramas, de gás oxigênio dissolvido foi igual a:
Ao final da mortandade, a quantidade consumida, em quilogramas, de gás oxigênio dissolvido foi igual a: