Questões de Vestibular UPE 2016 para Vestibular - 2º Dia
Foram encontradas 3 questões
Q1397374
Química
Uma cientista da Universidade de Ohio nos Estados Unidos desenvolveu um sistema para
transformar urina em combustível. A premissa parece simples e se baseia na decomposição da
amônia e da ureia. A imersão de um eletrodo no líquido e a aplicação de uma corrente suave no
sistema produzem uma substância que pode ser usada para alimentar uma célula de combustível.
Adaptado de: http://noticias.uol.com.br/ciencia/ultimas-noticias/bbc/2016/06/12/ (Acesso em: 20/06/2016)
A seguir, são feitas algumas afirmações sobre possíveis vantagens do sistema.
I. O gás nitrogênio produzido nessa eletrólise é um combustível menos poluente que o hidrogênio.
II. A ureia é decomposta em amônia que é vaporizada no sistema, antes de seguir para alimentar uma célula onde o gás é utilizado como combustível.
III. A energia fornecida para a produção do combustível pode ser menor que a utilizada na eletrólise da água, pois as ligações entre os átomos de hidrogênio e nitrogênio são mais fracas que as ligações entre os átomos da água.
Está CORRETO o que se afirma, apenas, em
Adaptado de: http://noticias.uol.com.br/ciencia/ultimas-noticias/bbc/2016/06/12/ (Acesso em: 20/06/2016)
A seguir, são feitas algumas afirmações sobre possíveis vantagens do sistema.
I. O gás nitrogênio produzido nessa eletrólise é um combustível menos poluente que o hidrogênio.
II. A ureia é decomposta em amônia que é vaporizada no sistema, antes de seguir para alimentar uma célula onde o gás é utilizado como combustível.
III. A energia fornecida para a produção do combustível pode ser menor que a utilizada na eletrólise da água, pois as ligações entre os átomos de hidrogênio e nitrogênio são mais fracas que as ligações entre os átomos da água.
Está CORRETO o que se afirma, apenas, em
Q1397378
Química
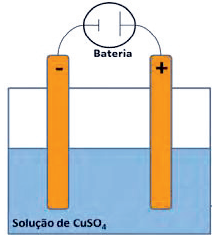
Para a produção de fios elétricos, o cobre deve possuir 99,9% de
pureza. Para tanto, o cobre metalúrgico (impuro) passa por um
processo, que gera o cobre eletrolítico, conforme está ilustrado na
figura ao lado.
Sobre esse processo, são feitas as afirmações a seguir:
I. No catodo (–), que é o cobre puro, ocorre depósito de mais cobre em virtude da redução do Cu2+ .
II. A corrosão faz a solução aumentar a concentração de Cu2+, que é atraído para o catodo, formando cobre metálico livre das impurezas.
III. Uma solução aquosa de NiSO4 aumentaria a deposição de cobre puro no catodo.
IV. No anodo (+), existe a oxidação do cobre metálico.
 Adaptado de:
http://www.acervodigital.unesp.br/bitstream/
123456789/46363/4/2ed_qui_m4d7.pdf
Adaptado de:
http://www.acervodigital.unesp.br/bitstream/
123456789/46363/4/2ed_qui_m4d7.pdf
Está CORRETO, apenas, o que se afirma em
Sobre esse processo, são feitas as afirmações a seguir:
I. No catodo (–), que é o cobre puro, ocorre depósito de mais cobre em virtude da redução do Cu2+ .
II. A corrosão faz a solução aumentar a concentração de Cu2+, que é atraído para o catodo, formando cobre metálico livre das impurezas.
III. Uma solução aquosa de NiSO4 aumentaria a deposição de cobre puro no catodo.
IV. No anodo (+), existe a oxidação do cobre metálico.
 Adaptado de:
http://www.acervodigital.unesp.br/bitstream/
123456789/46363/4/2ed_qui_m4d7.pdf
Adaptado de:
http://www.acervodigital.unesp.br/bitstream/
123456789/46363/4/2ed_qui_m4d7.pdf Está CORRETO, apenas, o que se afirma em
Q1397381
Química
Um fio de cobre foi retorcido em formato de uma “árvore de natal” e colocado dentro de um
béquer. Em seguida, transferiu-se um volume de uma solução salina para a vidraria, o suficiente para
cobrir o objeto metálico. Após determinado período, a solução ficou azulada, e pequenos cristais
cobriram toda a superfície da árvore de natal.

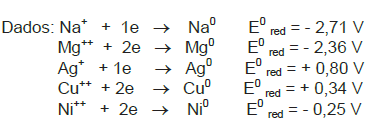
Qual é o sal presente na solução adicionada ao béquer?

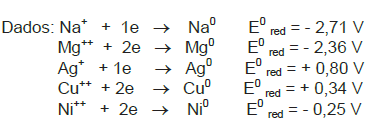
Qual é o sal presente na solução adicionada ao béquer?