Questões de Vestibular UNESP 2016 para Vestibular - Primeiro Semestre
Foram encontradas 7 questões
Ano: 2016
Banca:
VUNESP
Órgão:
UNESP
Prova:
VUNESP - 2016 - UNESP - Vestibular - Primeiro Semestre |
Q809377
Química
Analise o quadro 1, que apresenta diferentes soluções
aquosas com a mesma concentração em mol/L e à mesma
temperatura.
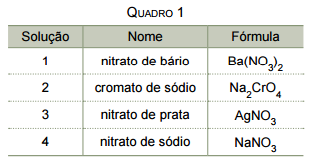
O quadro 2 apresenta o resultado das misturas, de volumes iguais, de cada duas dessas soluções.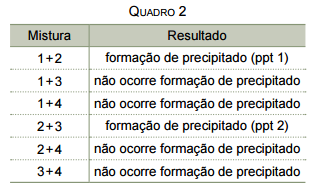
De acordo com essas informações, os precipitados formados, ppt 1 e ppt 2, são, respectivamente,

O quadro 2 apresenta o resultado das misturas, de volumes iguais, de cada duas dessas soluções.

De acordo com essas informações, os precipitados formados, ppt 1 e ppt 2, são, respectivamente,
Ano: 2016
Banca:
VUNESP
Órgão:
UNESP
Prova:
VUNESP - 2016 - UNESP - Vestibular - Primeiro Semestre |
Q809378
Química
O esquema representa um calorímetro utilizado para a
determinação do valor energético dos alimentos.
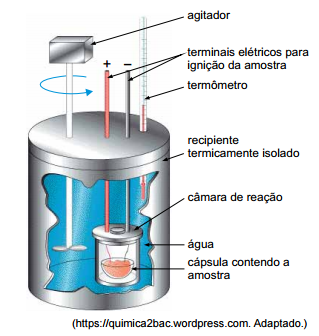
A tabela nutricional de determinado tipo de azeite de oliva traz a seguinte informação: “Uma porção de 13 mL (1 colher de sopa) equivale a 108 kcal.” Considere que o calor específico da água seja 1 kcal · kg–1 · ºC–1 e que todo o calor liberado na combustão do azeite seja transferido para a água. Ao serem queimados 2,6 mL desse azeite, em um calorímetro contendo 500 g de água inicialmente a 20,0 ºC e à pressão constante, a temperatura da água lida no termômetro deverá atingir a marca de

A tabela nutricional de determinado tipo de azeite de oliva traz a seguinte informação: “Uma porção de 13 mL (1 colher de sopa) equivale a 108 kcal.” Considere que o calor específico da água seja 1 kcal · kg–1 · ºC–1 e que todo o calor liberado na combustão do azeite seja transferido para a água. Ao serem queimados 2,6 mL desse azeite, em um calorímetro contendo 500 g de água inicialmente a 20,0 ºC e à pressão constante, a temperatura da água lida no termômetro deverá atingir a marca de
Ano: 2016
Banca:
VUNESP
Órgão:
UNESP
Prova:
VUNESP - 2016 - UNESP - Vestibular - Primeiro Semestre |
Q809379
Química
Em um experimento, um estudante realizou, nas Condições
Ambiente de Temperatura e Pressão (CATP), a
eletrólise de uma solução aquosa de ácido sulfúrico,
utilizando uma fonte de corrente elétrica contínua de
0,200 A durante 965 s. Sabendo que a constante de
Faraday é 96 500 C/mol e que o volume molar de gás
nas CATP é 25 000 mL/mol, o volume de H2
(g) desprendido
durante essa eletrólise foi igual a
Ano: 2016
Banca:
VUNESP
Órgão:
UNESP
Prova:
VUNESP - 2016 - UNESP - Vestibular - Primeiro Semestre |
Q809380
Química
O número total de átomos de hidrogênio presentes na
estrutura do gluconato de cálcio é
Ano: 2016
Banca:
VUNESP
Órgão:
UNESP
Prova:
VUNESP - 2016 - UNESP - Vestibular - Primeiro Semestre |
Q809381
Química
Considere que a constante de Avogadro seja 6,0 × 1023 mol–1
e que uma pessoa receba uma dose de 10 mL de uma
solução injetável de gluconato de cálcio a 10%. O número
total de íons Ca2+ que entrará no organismo dessa pessoa
após ela receber essa dose será
