Questões do Enem
Foram encontradas 112 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Um marceneiro esqueceu um pacote de pregos ao relento, expostos à umidade do ar e à chuva. Com isso, os pregos de ferro, que tinham a massa de 5,6 g cada, acabaram cobertos por uma camada espessa de ferrugem (Fe2O3 ˑ H2O), uma substância marrom insolúvel, produto da oxidação do ferro metálico, que ocorre segundo a equação química:
2 Fe (s) + 3/2 O2 (g) + H2O (l) → Fe2O3 ˑ H2O (s)
Qual foi a massa de ferrugem produzida ao se oxidar a
metade (50%) de um prego?
Uma antiga forma de produzir um dos constituintes de argamassas é o aquecimento a altas temperaturas de materiais componentes dos sambaquis, que são sítios arqueológicos formados essencialmente por restos de moluscos. A decomposição térmica da principal substância desses sítios arqueológicos resulta na formação de dois compostos apenas. Um deles é um óxido sólido e o outro é um óxido gasoso. A reação do primeiro com água resulta na formação de Ca(OH)2 (aquoso), enquanto a reação do segundo resulta em H2CO3 (aquoso).
A fórmula da principal substância encontrada nesses sítios arqueológicos é:
A presença de substâncias ricas em enxofre em áreas de mineração provoca preocupantes impactos ambientais. Um exemplo dessas substâncias é a pirita (FeS2), que, em contato com o oxigênio atmosférico, reage formando uma solução aquosa ferruginosa, conhecida como drenagem ácida de minas, segundo a equação química:
4 FeS2 (s) + 15 O2 (g) + 2 H2O (l) → 2 Fe2 (SO4 )3 (aq) + 2 H2SO4 (aq)
Em situações críticas, nas quais a concentração do ácido sulfúrico atinge 9,8 g/L, o pH alcança valores menores que 1,0. Uma forma de reduzir o impacto da drenagem ácida de minas é tratá-la com calcário (CaCO3). Considere que uma amostra comercial de calcário, com pureza igual a 50% em massa, foi disponibilizada para o tratamento.
FIGUEIREDO, B. R. Minérios e ambientes. Campinas: Unicamp, 2000 (adaptado).
Qual é a massa de calcário, em gramas, necessária para neutralizar um litro de drenagem ácida de minas, em
seu estado crítico, sabendo-se que as massas molares do CaCO3 e do H2SO4 são iguais a 100 g/mol e 98 g/mol,
respectivamente?
As plantas realizam fotossíntese pela captura do gás carbônico atmosférico e, juntamente com a água e a luz solar, produzem os carboidratos. No esquema está apresentada a equação desse processo, em que as letras x e y representam os coeficientes estequiométricos da reação.
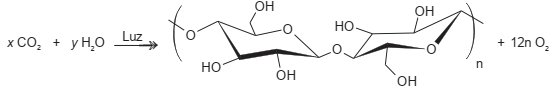
Quais são os valores dos coeficientes x e y da equação balanceada de produção do carboidrato e oxigênio?
O ácido sulfúrico (H2SO4 ) é um dos ácidos mais utilizados em indústrias e em laboratórios. O resíduo ácido gerado pelo seu uso pode provocar sérios danos ao meio ambiente. Em um laboratório, gerou-se uma grande quantidade de resíduo ácido a partir do ácido sulfúrico, o qual necessita ser neutralizado para o seu descarte. O técnico desse laboratório tem à sua disposição cinco substâncias: CaO, K2SO4 , NaHSO4 , CH3CH2OH e C5H9CONH2 .
Qual dessas substâncias é a adequada para realizar esse tratamento?