Questões Militares de Química - Substâncias Inorgânicas e suas características: Ácidos, Bases, Sais e Óxidos. Reações de Neutralização.
Foram encontradas 118 questões
Q2463540
Química
Texto associado
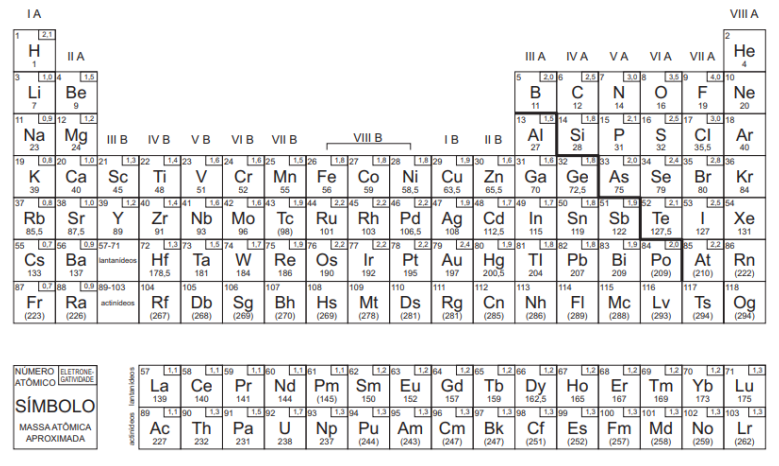
Atenção! A tabela periódica a seguir servirá de apoio a questão da prova de Química.

Atualmente é difícil imaginar a vida sem o uso de smartphones.
Estes pequenos dispositivos têm desempenhado cada vez mais
funções, que vão muito além de fazer e receber chamadas.
No entanto, apesar de pequenos, estes aparelhos demandam uma grande quantidade de elementos químicos na sua confecção. Observe o quadro a seguir, que apresenta alguns dos elementos que compõem as diferentes partes do aparelho.
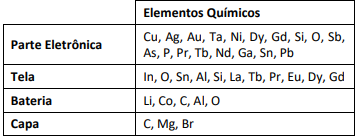
A partir da composição química apresentada no quadro, avalie as seguintes afirmativas:
I. A parte eletrônica é constituída somente por metais.
II. Na tela estão presentes seis elementos de transição interna.
III. Os elementos presentes na bateria pertencem ao segundo período da classificação periódica.
IV. A capa é constituída por elementos representativos.
Está correto apenas o que se afirma em
No entanto, apesar de pequenos, estes aparelhos demandam uma grande quantidade de elementos químicos na sua confecção. Observe o quadro a seguir, que apresenta alguns dos elementos que compõem as diferentes partes do aparelho.

A partir da composição química apresentada no quadro, avalie as seguintes afirmativas:
I. A parte eletrônica é constituída somente por metais.
II. Na tela estão presentes seis elementos de transição interna.
III. Os elementos presentes na bateria pertencem ao segundo período da classificação periódica.
IV. A capa é constituída por elementos representativos.
Está correto apenas o que se afirma em
Ano: 2024
Banca:
CESPE / CEBRASPE
Órgão:
CBM-PA
Prova:
CESPE / CEBRASPE - 2024 - CBM-PA - Oficial do Corpo de Bombeiros |
Q2350506
Química
Assinale a opção que apresenta correta a ordem decrescente de
força dos oxiácidos HBrO, HBrO2, HBrO3 e HBrO4.
Q2280185
Química
Considere 1 L de solução aquosa preparada por meio da adição de 1 mol de
um ácido monoprótico hipotético, 1 mol de sua base conjugada e 0,82 mol de uma base
forte. Sabendo que a constante de ionização do ácido é igual a 10-4, assinale a alternativa
que melhor representa o pH da solução resultante.
Q2280184
Química
Considere as seguintes afirmações relacionadas à ocorrência ou não de
reações químicas em condições ambientes.
I. Ao borbulhar gás cloro em uma solução aquosa de iodeto de sódio, haverá a formação
de um sólido.
II. Ao borbulhar gás cloro em uma solução aquosa e incolor de brometo de sódio, a solução se tornará ligeiramente marrom.
III. Ao adicionar uma solução aquosa de iodeto de sódio a uma solução aquosa de cloreto de potássio, haverá a formação de um gás.
IV. Ao adicionar bromo líquido a uma solução aquosa de fluoreto de sódio, haverá formação de um gás.
V. Ao adicionar bromo líquido a uma solução aquosa de iodeto de sódio, haverá formação de um sólido.
II. Ao borbulhar gás cloro em uma solução aquosa e incolor de brometo de sódio, a solução se tornará ligeiramente marrom.
III. Ao adicionar uma solução aquosa de iodeto de sódio a uma solução aquosa de cloreto de potássio, haverá a formação de um gás.
IV. Ao adicionar bromo líquido a uma solução aquosa de fluoreto de sódio, haverá formação de um gás.
V. Ao adicionar bromo líquido a uma solução aquosa de iodeto de sódio, haverá formação de um sólido.
Das afirmações acima, estão CORRETAS
Ano: 2023
Banca:
VUNESP
Órgão:
EsFCEx
Prova:
VUNESP - 2023 - EsFCEx - Oficial - Magistério em Química |
Q2260535
Química
Texto associado
A maior parte da produção industrial do magnésio é obtida a partir da água do mar, onde o elemento químico
magnésio se encontra na forma de íons Mg2+
(aq), em
concentração média de 1,3 g.L–1
. O processo segue as
seguintes etapas:
I. Precipitação de Mg(OH)2 por adição de cal viva.
II. Conversão a MgCl2 por adição de HCl.
III. Eletrólise ígnea do MgCl2.
Sabendo que o HCl concentrado (pró-análise) tem densidade 1,18 g.cm3
e concentração de 37% em massa, a
neutralização de 1,0 kg de Mg(OH)2
(s) vai consumir um
volume de HCl concentrado de, aproximadamente,