Questões de Concurso Militar EsPCEx 2015 para Cadete do Exército - 1° Dia
Foram encontradas 12 questões
Ano: 2015
Banca:
Exército
Órgão:
EsPCEx
Prova:
Exército - 2015 - EsPCEx - Cadete do Exército - 1° Dia |
Q616489
Química
A nitroglicerina é um líquido oleoso de cor amarelo-pálida, muito sensível ao choque ou calor. É empregada em diversos tipos de explosivos. Sua reação de decomposição inicia-se facilmente e gera rapidamente grandes quantidades de gases, expressiva força de expansão e intensa liberação de calor, conforme a equação da reação: 4 C3H5N3O9 (l) ➝ 6 N2 (g) + 12 CO2 (g) + 10 H2O (g) + O2 (g)
Admitindo-se os produtos gasosos da reação como gases ideais, cujos volumes molares são iguais a 24,5 L, e tomando por base a equação da reação de decomposição da nitroglicerina, o volume total aproximado, em litros, de gases produzidos na reação de decomposição completa de 454 g de nitroglicerina será de
Dados: massa molar da nitroglicerina = 227 g/mol; volume molar = 24,5 L/mol (25 ºC e 1 atm)
Dados: massa molar da nitroglicerina = 227 g/mol; volume molar = 24,5 L/mol (25 ºC e 1 atm)
Ano: 2015
Banca:
Exército
Órgão:
EsPCEx
Prova:
Exército - 2015 - EsPCEx - Cadete do Exército - 1° Dia |
Q616490
Química
Um químico trabalhando em seu laboratório resolveu preparar uma solução de hidróxido de sódio (NaOH) numa concentração adequada, para posterior utilização em análises titulométricas. Consultando seu estoque verificou a existência de uma solução de NaOH de concentração 0,01 mol·L-1, inadequada a seus propósitos. Para a preparação da solução de NaOH na concentração adequada, pipetou dez mililitros (10 mL) dessa solução aquosa de NaOH estocada e, em seguida, transferiu o volume pipetado para um balão volumétrico de 1000 mL de capacidade, completando seu volume com água pura. Considerando que o experimento ocorreu nas condições de 25 °C e 1 atm e que o hidróxido de sódio se encontrava completamente dissociado, o pH dessa solução resultante final preparada pelo Químico será:
Ano: 2015
Banca:
Exército
Órgão:
EsPCEx
Prova:
Exército - 2015 - EsPCEx - Cadete do Exército - 1° Dia |
Q616491
Química
O composto representado pela fórmula estrutural, abaixo, pertence à função orgânica dos ácidos carboxílicos e apresenta alguns substituintes orgânicos, que correspondem a uma ramificação como parte de uma cadeia carbônica principal, mas, ao serem mostrados isoladamente, como estruturas que apresentam valência livre, são denominados radicais. (Texto adaptado de: Fonseca, Martha Reis Marques da, Química: química orgânica, pág 33, FTD, 2007).
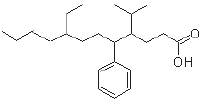
O nome dos substituintes orgânicos ligados respectivamente aos carbonos de número 4, 5 e 8 da cadeia principal, são

O nome dos substituintes orgânicos ligados respectivamente aos carbonos de número 4, 5 e 8 da cadeia principal, são
Ano: 2015
Banca:
Exército
Órgão:
EsPCEx
Prova:
Exército - 2015 - EsPCEx - Cadete do Exército - 1° Dia |
Q616492
Química
Compostos iônicos são aqueles que apresentam ligação iônica. A ligação iônica é a ligação entre íons positivos e negativos, unidos por forças de atração eletrostática. (Texto adaptado de: Usberco, João e Salvador, Edgard, Química: química geral, vol 1, pág 225, Saraiva, 2009).
Sobre as propriedades e características de compostos iônicos são feitas as seguintes afirmativas: I – apresentam brilho metálico. II – apresentam elevadas temperaturas de fusão e ebulição. III – apresentam boa condutibilidade elétrica quando em solução aquosa. IV – são sólidos nas condições ambiente (25 °C e 1atm). V – são pouco solúveis em solventes polares como a água.
Das afirmativas apresentadas estão corretas apenas
Das afirmativas apresentadas estão corretas apenas
Ano: 2015
Banca:
Exército
Órgão:
EsPCEx
Prova:
Exército - 2015 - EsPCEx - Cadete do Exército - 1° Dia |
Q616493
Química
O dióxido de enxofre é um dos diversos gases tóxicos poluentes, liberados no ambiente por fornos de usinas e de indústrias. Uma das maneiras de reduzir a emissão deste gás tóxico é a injeção de carbonato de cálcio no interior dos fornos industriais. O carbonato de cálcio injetado nos fornos das usinas se decompõe formando óxido de cálcio e dióxido de carbono. O óxido de cálcio, então, reage com o dióxido de enxofre para formar o sulfito de cálcio no estado sólido, menos poluente.
Assinale a alternativa que apresenta, na sequência em que aparecem no texto (desconsiderando-se as repetições), as fórmulas químicas dos compostos, grifados e em itálico, mencionados no processo.