Questões Militares
Foram encontradas 237 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Q2280189
Química
As energias de ligação do H2, do Cl2 e do HCl nas condições padrão e a 25 °C,
em kJ mol-1, são 434, 243 e 431, respectivamente. Com base nessas informações, assinale
a alternativa que apresenta a entalpia padrão de formação do HCl, em kJ mol-1.
Ano: 2023
Banca:
VUNESP
Órgão:
EsFCEx
Prova:
VUNESP - 2023 - EsFCEx - Oficial - Magistério em Química |
Q2260544
Química
A mistura entre íons permanganato e peróxido, em meio ácido, pode ser representada pela seguinte equação não balanceada:
MnO4 – (aq) + H2 O2 (aq) + H+ (aq) → Mn2+ (aq) + O2 (g) + H2 O(l)
Considerando as semirreações e seus potenciais de redução, a 25 ºC,
O2 + 2 H+ + 2 e– → H2 O2 ; E0 = + 0,68 V MnO4 – (aq) + 8 H+ (aq) + 5 e– → Mn2+(aq) + 4 H2 O(l); E0 = +1,51 V
conclui-se que o potencial da reação global e os coeficientes estequiométricos menores e inteiros que completam a equação são:
MnO4 – (aq) + H2 O2 (aq) + H+ (aq) → Mn2+ (aq) + O2 (g) + H2 O(l)
Considerando as semirreações e seus potenciais de redução, a 25 ºC,
O2 + 2 H+ + 2 e– → H2 O2 ; E0 = + 0,68 V MnO4 – (aq) + 8 H+ (aq) + 5 e– → Mn2+(aq) + 4 H2 O(l); E0 = +1,51 V
conclui-se que o potencial da reação global e os coeficientes estequiométricos menores e inteiros que completam a equação são:
Ano: 2023
Banca:
VUNESP
Órgão:
EsFCEx
Prova:
VUNESP - 2023 - EsFCEx - Oficial - Magistério em Química |
Q2260538
Química
O sulfeto de hidrogênio é naturalmente oxidado pelo oxigênio do ar, conforme a reação representada a seguir:
2 H2 S(g) + 3 O2 (g) → 2 SO2 (g) + 2 H2 O(g)
A tabela reúne as entalpias de formação dos componentes da reação.

Portanto, a entalpia da reação, em kJ.mol–1 de H2 S(g), é, aproximadamente,
2 H2 S(g) + 3 O2 (g) → 2 SO2 (g) + 2 H2 O(g)
A tabela reúne as entalpias de formação dos componentes da reação.

Portanto, a entalpia da reação, em kJ.mol–1 de H2 S(g), é, aproximadamente,
Ano: 2023
Banca:
VUNESP
Órgão:
EsFCEx
Prova:
VUNESP - 2023 - EsFCEx - Oficial - Magistério em Química |
Q2260526
Química
A reação do sódio metálico com etanol é uma forma mais
segura de eliminação de resíduos do metal, quando comparada sua reação com a água, e pode ser representada
pela equação não balanceada:
Na + CH3 CH2 OH → CH3 CH2 ONa + H2
Considerando que nas CATP (Condições Ambientais de Temperatura e Pressão) 1 mol de qualquer gás ocupa 25 L, o volume de H2 produzido, quando reagem 1 g de sódio e 1 g etanol, e a massa do excesso de reagente são, respectivamente,
Na + CH3 CH2 OH → CH3 CH2 ONa + H2
Considerando que nas CATP (Condições Ambientais de Temperatura e Pressão) 1 mol de qualquer gás ocupa 25 L, o volume de H2 produzido, quando reagem 1 g de sódio e 1 g etanol, e a massa do excesso de reagente são, respectivamente,
Q2101627
Química
No dia 09 de maio de 2015, por volta das 13h, a
equipe do Corpo de Bombeiros foi acionada para
ocorrência de desabamento de uma ponte no
Município de Pedra Branca. Mais de 20 cavalos
morreram e 4 pessoas ficaram feridas. Com o
auxílio da equipe de mergulho do Corpo de
Bombeiros, os animais mortos foram removidos.
Segundo o laudo do Conselho Regional de
Engenharia e Agronomia de Sergipe, a corrosão
dos cabos metálicos de sustentação foi a causa do
desabamento da ponte. Considerando os processos
eletroquímicos, analise as informações a seguir.
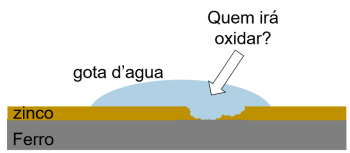
Considerando a imagem e os valores de E°red fornecidos, é CORRETO afirmar que a substância que sofrerá oxidação será:

Considerando a imagem e os valores de E°red fornecidos, é CORRETO afirmar que a substância que sofrerá oxidação será: