Questões de Vestibular de Química - Eletroquímica: Oxirredução, Potenciais Padrão de Redução, Pilha, Eletrólise e Leis de Faraday.
Foram encontradas 70 questões
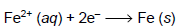
Considerando a Constante de Faraday = 96 500 C/mol, 1 hora = 3 600 s e massa molar do ferro (Fe) = 56 g/mol, a massa aproximada de ferro metálico que pode ser depositada no cátodo, nessas condições, é
C6(s) + Li+ (PC) + e- → LiC6(s) E° = 0,855 V
CoO2(s) + Li+ (PC) + e- → LiCoO2(s) E° = - 2,745 V
Baseado nos dados acima, qual a equação global e o potencial da pilha?
De acordo com os potenciais de redução descritos abaixo, em qual(is) recipiente(s) será possível armazenar a solução de CuSO4, sem que ocorram reações químicas redox espontâneas?
Zn2+(aq) + 2e- → Zn(s) - 0,76 V Fe2+(aq) + 2e- → Fe(s) - 0,44 V Ni2+(aq) + 2e- → Ni(s) - 0,25 V Cu2+(aq) + 2e- → Cu(s) + 0,34 V Ag+ (aq) + e- → Ag(s) + 0,80 V
Admita uma solução aquosa de sulfato de ferro(II) que passou por um processo de eletrólise durante duas horas, empregando-se uma corrente elétrica com intensidade (i) de 5 A, e a semirreação a seguir:
Fe2 + (aq) + 2e- → Fe(s)
Considerando a Constante de Faraday = 96 500 C/mol, 1 hora = 3 600 s e massa molar do ferro (Fe) = 56 g/mol, a massa aproximada de ferro metálico que pode ser depositada no cátodo, nessas condições, é
Dados: Mn +2 + 2e ⇾ Mnº Eº = -1,18v Zn +2 + 2e º ⇾ Znº Eº = -0,76v