Questões de Vestibular de Química - Eletroquímica: Oxirredução, Potenciais Padrão de Redução, Pilha, Eletrólise e Leis de Faraday.
Foram encontradas 71 questões

Numa dada combinação para montar uma pilha eletroquímica, o valor de diferença de potencial (AE) da pilha, no instante em que se ligaram os contatos, foi de 0,69 V.
A combinação utilizada nessa pilha foi entre as semicélulas:
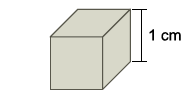
Deseja-se recobrir as faces desse cubo com uma camada uniforme de cobre de 1 × 10–2 cm de espessura. Para isso, o cubo pode ser utilizado como cátodo de uma cuba eletrolítica contendo íons Cu2+(aq). Admita que a eletrólise se realize sob corrente elétrica de 200 mA, que a constante de Faraday seja igual a 1 × 105 C/mol e que a densidade do cobre seja 9 g/cm3 . Assim, estima-se que o tempo de eletrólise necessário para que se deposite no cubo a camada de cobre desejada será próximo de
I. É a aplicação de uma camada de cobre ou ligas de cobre sobre a superfície de aço ou ferro.
II. A finalidade da galvanização é formar uma capa protetora que evite a corrosão do metal.
III. O método mais usado de galvanização é o de imersão a quente.
IV. O metal utilizado na galvanização é conhecido como metal de sacrifício e tem maior poder de redução que o metal a ser protegido.
São verdadeiras somente as proposições
Co+2 + 2e- → Co(s) Eº = - 0.28 V
4e- + O2 (g) + 4 H+ → 2H2O Eº = 1.23V
Após a passagem, pela célula, de uma corrente de 5.0 A durante 1.5 h, as massas de cobalto metálico e de gás oxigênio produzidas são, respectivamente:
