Questões de Vestibular de Química - Termoquímica: Energia Calorífica, Calor de reação, Entalpia, Equações e Lei de Hess.
Foram encontradas 338 questões
Q1797131
Química
Na medicina veterinária, o cloreto de amônio (NH4Cl) é
utilizado como acidulante da urina com o objetivo de
evitar infecções. Para a produção do NH4Cl, é
empregada a reação do ácido clorídrico (HCl) com
amônia (NH3), representada abaixo:
HCl(aq) + NH3(aq) → NH4Cl(s)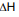 = ???
= ???
A partir dos valores das entalpias de formação do HCl ( = -46 kJ.mol-1), NH3 (
= -46 kJ.mol-1), NH3 ( = -92 kJ.mol-1) e NH4Cl (
= -92 kJ.mol-1) e NH4Cl ( = -314 kJ.mol-1), determine a variação de entalpia
(
= -314 kJ.mol-1), determine a variação de entalpia
(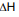 ) da reação acima e se o processo é endotérmico
ou exotérmico.
) da reação acima e se o processo é endotérmico
ou exotérmico.
HCl(aq) + NH3(aq) → NH4Cl(s)
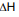 = ???
= ??? A partir dos valores das entalpias de formação do HCl (
 = -46 kJ.mol-1), NH3 (
= -46 kJ.mol-1), NH3 ( = -92 kJ.mol-1) e NH4Cl (
= -92 kJ.mol-1) e NH4Cl ( = -314 kJ.mol-1), determine a variação de entalpia
(
= -314 kJ.mol-1), determine a variação de entalpia
(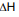 ) da reação acima e se o processo é endotérmico
ou exotérmico.
) da reação acima e se o processo é endotérmico
ou exotérmico.
Ano: 2021
Banca:
PUC-MINAS
Órgão:
PUC-MINAS
Prova:
PUC-MINAS - 2021 - PUC-MINAS - Vestibular Medicina - Caderno 1 |
Q1796708
Química
O Ciclo de Born-Haber é uma proposta para analisar a energia envolvida numa reação e foi
desenvolvido em 1917 pelos cientistas alemães Max Born e Fritz Haber.
Esse ciclo envolve a formação de um composto iônico a partir da reação de um metal com um ametal. É
utilizado, principalmente, como um método para calcular a entalpia reticular, a qual não pode ser
mensurada diretamente.
Considere o ciclo para o NaCl na figura a seguir:
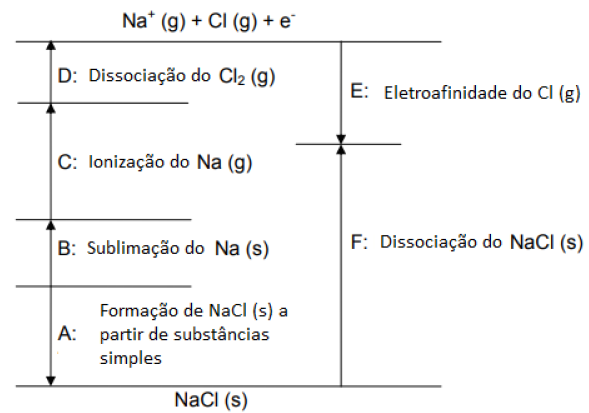
A representação CORRETA de um dos processos que ocorrem nesse ciclo é:
Considere o ciclo para o NaCl na figura a seguir:

A representação CORRETA de um dos processos que ocorrem nesse ciclo é:
Ano: 2021
Banca:
PUC-MINAS
Órgão:
PUC-MINAS
Prova:
PUC-MINAS - 2021 - PUC-MINAS - Vestibular Medicina - Caderno 1 |
Q1796706
Química
A Lei de Hess diz que a variação de entalpia envolvida em uma reação química, sob certas condições
experimentais, depende exclusivamente da entalpia inicial e final dos produtos, seja a reação executada
diretamente em uma única etapa ou indiretamente, em uma série de etapas.
Considere o gráfico a seguir:
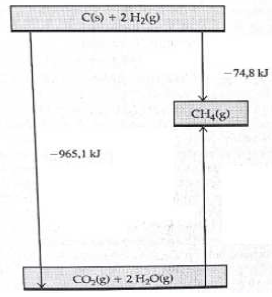
A energia envolvida na formação do gás metano a partir de gás carbônico e água é:

A energia envolvida na formação do gás metano a partir de gás carbônico e água é:
Ano: 2018
Banca:
COTEC
Órgão:
Unimontes - MG
Prova:
COTEC - 2018 - Unimontes - MG - Vestibular Paes - 3º Etapa |
Q1794780
Química
De acordo com a lei de Hess, a variação de total de entalpia, ∆Hº, de um processo depende somente das
energias dos estados inicial e final, e não do caminho seguido. Assim, a entalpia de formação, ∆Hºf
, é igual
à soma das demais entalpias que aparecem no ciclo do cloreto de sódio.
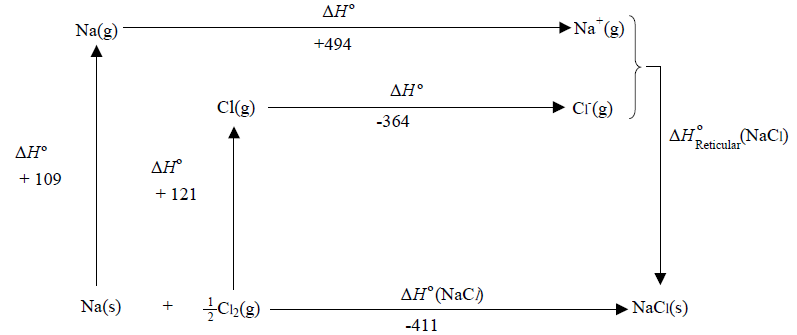
Considerando a relação da energia reticular, U ou ∆Hºreticular, do cloreto de sódio com outros dados termoquímicos, é CORRETO afirmar que, para

Considerando a relação da energia reticular, U ou ∆Hºreticular, do cloreto de sódio com outros dados termoquímicos, é CORRETO afirmar que, para
Ano: 2019
Banca:
Universidade Presbiteriana Mackenzie
Órgão:
MACKENZIE
Prova:
Universidade Presbiteriana Mackenzie - 2019 - MACKENZIE - Vestibular Mackenzie - Grupos II e III |
Q1793889
Química
A reação de Sabatier-Senderens é um tipo de reação de adição, na qual átomos
de hidrogênio são acrescentados aos carbonos unidos por uma ligação dupla, na
presença de um catalisador, produzindo um alcano correspondente. Considerandose que o but-2-eno seja submetido a esse processo, bem como os valores das
energias de ligação, dadas na tabela abaixo, é correto afirmar que a variação
da entalpia dessa reação, expressa em kJ∙mol-1, efetuada no estado padrão, é de



