Questões Militares de Química - Grandezas: massa, volume, mol, massa molar, constante de Avogadro e Estequiometria.
Foram encontradas 193 questões
Q2463541
Química
Texto associado
Atenção! A tabela periódica a seguir servirá de apoio a questão da prova de Química.

Em um determinado processo de análise duas amostras
hipotéticas (A e B) foram estudadas por meio de diversos
experimentos.
O gráfico a seguir apresenta os resultados obtidos para a relação entre massa e volume de cada uma dessas amostras, medidos a 25ºC.
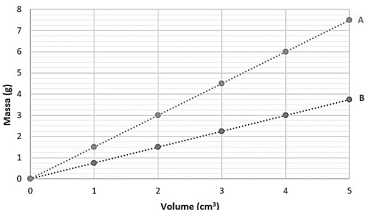
A partir dos dados apresentados é possível afirmar que, nessa temperatura, a razão entre as densidades das amostras A e B é igual a
O gráfico a seguir apresenta os resultados obtidos para a relação entre massa e volume de cada uma dessas amostras, medidos a 25ºC.

A partir dos dados apresentados é possível afirmar que, nessa temperatura, a razão entre as densidades das amostras A e B é igual a
Q2280178
Química
Considere as afirmações a respeito da reação de combustão completa de
misturas estequiométricas, nas condições ambientes.
I. Em uma mistura de hidrogênio e oxigênio, o combustível representa aproximadamente
11% da massa total.
II. Em uma mistura de octano e oxigênio, o combustível representa aproximadamente 78% da massa total.
III. A variação de temperatura da reação de combustível e oxigênio (por mol de combustível) é igual à variação de temperatura da reação de combustível e ar atmosférico (por mol de combustível).
IV. A entalpia molar de combustão de uma mistura de combustível e oxigênio é igual à entalpia molar de combustão de uma mistura de combustível e ar atmosférico. Assinale a opção que contém as afirmações CORRETAS.
II. Em uma mistura de octano e oxigênio, o combustível representa aproximadamente 78% da massa total.
III. A variação de temperatura da reação de combustível e oxigênio (por mol de combustível) é igual à variação de temperatura da reação de combustível e ar atmosférico (por mol de combustível).
IV. A entalpia molar de combustão de uma mistura de combustível e oxigênio é igual à entalpia molar de combustão de uma mistura de combustível e ar atmosférico. Assinale a opção que contém as afirmações CORRETAS.
Ano: 2023
Banca:
VUNESP
Órgão:
EsFCEx
Prova:
VUNESP - 2023 - EsFCEx - Oficial - Magistério em Química |
Q2260526
Química
A reação do sódio metálico com etanol é uma forma mais
segura de eliminação de resíduos do metal, quando comparada sua reação com a água, e pode ser representada
pela equação não balanceada:
Na + CH3 CH2 OH → CH3 CH2 ONa + H2
Considerando que nas CATP (Condições Ambientais de Temperatura e Pressão) 1 mol de qualquer gás ocupa 25 L, o volume de H2 produzido, quando reagem 1 g de sódio e 1 g etanol, e a massa do excesso de reagente são, respectivamente,
Na + CH3 CH2 OH → CH3 CH2 ONa + H2
Considerando que nas CATP (Condições Ambientais de Temperatura e Pressão) 1 mol de qualquer gás ocupa 25 L, o volume de H2 produzido, quando reagem 1 g de sódio e 1 g etanol, e a massa do excesso de reagente são, respectivamente,
Q2210686
Química
A perovskita CH3NH3PbI3 é um material que, pelas suas propriedades fotovoltaicas, é considerado promissor para
geração de eletricidade a partir da luz solar. O composto foi sintetizado em três etapas, descritas pelas equações
químicas a seguir.
Pb(NO3)2 + 2KI → PbI2 + 2KNO3 CH3NH2 + HI → CH3NH3I PbI2 + CH3NH3I → CH3NH3PbI3
Os seguintes reagentes foram empregados na síntese: 0,6 mol de Pb(NO3)2; 0,8 mol de KI; 0,7 mol de CH3NH2; e 0,8 mol de HI. Nessas condições, qual será a quantidade máxima da perovskita CH3NH3PbI3 produzida?
Pb(NO3)2 + 2KI → PbI2 + 2KNO3 CH3NH2 + HI → CH3NH3I PbI2 + CH3NH3I → CH3NH3PbI3
Os seguintes reagentes foram empregados na síntese: 0,6 mol de Pb(NO3)2; 0,8 mol de KI; 0,7 mol de CH3NH2; e 0,8 mol de HI. Nessas condições, qual será a quantidade máxima da perovskita CH3NH3PbI3 produzida?
Ano: 2022
Banca:
INSTITUTO AOCP
Órgão:
CBM-GO
Prova:
INSTITUTO AOCP - 2022 - CBM-GO - Aspirante do Corpo de Bombeiros |
Q2154912
Química
Uma operação realizada pelo Corpo de
Bombeiros, a fim de impedir um grave acidente
em uma caldeira de uma indústria de bebidas,
possibilitou revelar que a água que alimentava a
caldeira apresentou um índice de dureza de 250
ppm (partes por milhão) de CaCO3. Considerando
que a densidade da solução (amostra) é 1 g/cm3
, é
correto afirmar que