Questões Militares de Química - Grandezas: massa, volume, mol, massa molar, constante de Avogadro e Estequiometria.
Foram encontradas 193 questões
Q2070343
Química
Após o derramamento de grande volume de
ácido sulfúrico concentrado em um
laboratório, o Corpo de Bombeiros foi
acionado para isolar o local. Para neutralizar
todo o ácido sulfúrico derramado, foi
colocado carbonato de cálcio sobre a área.
Considerando a reação balanceada entre o
ácido sulfúrico e o carbonato de cálcio,
assinale a alternativa que apresenta a soma
de todos os coeficientes estequiométricos,
com os menores números inteiros.
Ano: 2022
Banca:
IDECAN
Órgão:
CBM-MS
Prova:
IDECAN - 2022 - CBM-MS - Oficial do Corpo de Bombeiros Militar do Estado de Mato Grosso do Sul |
Q2059859
Química
O metanoato de sódio (HCOONa) é um composto utilizado na
indústria para a obtenção do ácido fórmico (HCOOH) por meio
de uma reação com ácido sulfúrico (H2SO4). A reação está
apresentada abaixo.
2. HCOONa + H2SO4 → 2HCOOH + Na2SO4
Uma solução aquosa foi preparada a partir da dissolução de 6,8 g de metanoato de sódio em 100 ml de água. Essa solução preparada reagiu com uma solução de ácido sulfúrico com centração de 0,2 mol/L para formação do ácido fórmico. Sabendo que a quantidade de solução de ácido sulfúrico foi a quantidade estequiométrica para completar a reação de síntese, a concentração da solução de metanoato de sódio preparada e a quantidade de solução de ácido sulfúrico adicionada, respectivamente, foram:
Massa molar: Na=23 g/mol; C=12 g/mol; O=12 g/mol; O=16 g/mol; H=1 g/mol
2. HCOONa + H2SO4 → 2HCOOH + Na2SO4
Uma solução aquosa foi preparada a partir da dissolução de 6,8 g de metanoato de sódio em 100 ml de água. Essa solução preparada reagiu com uma solução de ácido sulfúrico com centração de 0,2 mol/L para formação do ácido fórmico. Sabendo que a quantidade de solução de ácido sulfúrico foi a quantidade estequiométrica para completar a reação de síntese, a concentração da solução de metanoato de sódio preparada e a quantidade de solução de ácido sulfúrico adicionada, respectivamente, foram:
Massa molar: Na=23 g/mol; C=12 g/mol; O=12 g/mol; O=16 g/mol; H=1 g/mol
Q2029713
Química
A densidade não é uma forma de expressar
concentração. É comum encontrarmos densímetros
nos postos de gasolina, para auxiliar no controle de
qualidade da gasolina.
Sobre esse assunto, é correto afirmar que:
Sobre esse assunto, é correto afirmar que:
Q2024787
Química
O palito de fósforo é um dos artigos mais úteis no nosso cotidiano. Na sua composição, possui fósforo vermelho,
enxofre e clorato de potássio. A cabeça de um palito de fósforo pesa aproximadamente 0,05 g. A reação que ocorre na
queima da cabeça de fósforo está representada a seguir:

O cheiro característico de “fósforo queimado” se deve ao dióxido de enxofre formado.
Dados: No palito de fósforo, os componentes estão em quantidades estequiométricas. M (g mol-1 ): Cl = 35,5; K = 39; O= 16; P = 31; S = 32.
A massa (em g) de dióxido de enxofre produzido ao queimar uma cabeça de fósforo é aproximadamente:

O cheiro característico de “fósforo queimado” se deve ao dióxido de enxofre formado.
Dados: No palito de fósforo, os componentes estão em quantidades estequiométricas. M (g mol-1 ): Cl = 35,5; K = 39; O= 16; P = 31; S = 32.
A massa (em g) de dióxido de enxofre produzido ao queimar uma cabeça de fósforo é aproximadamente:
Q2015282
Química
Em momentos de estresse, as glândulas suprarrenais secretam o hormônio
adrenalina, que, a partir da aceleração dos batimentos cardíacos, do aumento da
pressão arterial e da contração ou relaxamento de músculos, prepara o organismo
para a fuga ou para a defesa.
Dados – M (g mol-1 ): H = 1; C = 12; N = 14; O = 16.
Qual é o valor da massa molar (em g mol-1 ) desse composto?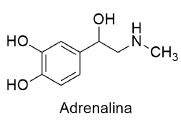
Dados – M (g mol-1 ): H = 1; C = 12; N = 14; O = 16.
Qual é o valor da massa molar (em g mol-1 ) desse composto?
